题目内容
【题目】下列说法正确的是
A. 蛋白质溶液中加入饱和硫酸铵溶液,蛋白质发生变性
B. 全降解塑料![]() 可由环氧丙烷
可由环氧丙烷![]() 和CO2缩聚制得
和CO2缩聚制得
C. 用牛油制肥皂,当在反应液中加入热的饱和食盐水并搅拌后,会发现烧杯底部有固体物质析出
D. 在用油脂制肥皂实验中,加入乙醇是为了增大油脂和NaOH 溶液的接触面积,从而加快化学反应速率
【答案】D
【解析】A.蛋白质遇到重金属盐会变性;B.环氧丙烷![]() 和CO2通过加聚制得全降解塑料;C.高级脂肪酸钠,该物质在饱和食盐水中溶解度较小,且密度小于水;D.油脂难溶于水,在乙醇中的溶解度较大。
和CO2通过加聚制得全降解塑料;C.高级脂肪酸钠,该物质在饱和食盐水中溶解度较小,且密度小于水;D.油脂难溶于水,在乙醇中的溶解度较大。
蛋白质溶液中加入饱和硫酸铵溶液,降低蛋白质的溶解度,属于蛋白质发生了盐析,物理变化,A错误;全降解塑料可由单体环氧丙烷![]() 和CO2通过加聚反应生成,B错误;牛油在碱性条件下水解生成高级脂肪酸钠,该物质在饱和食盐水中溶解度较小,且密度小于水,则析出的肥皂浮在上层而不是沉于液面底部,C错误;油脂难溶于水,在乙醇中的溶解度较大,油脂制肥皂实验中加入一定量的乙醇为了增大油脂的溶解,增大与NaOH 溶液的接触面积,从而加快化学反应速率,D正确;正确选项D。
和CO2通过加聚反应生成,B错误;牛油在碱性条件下水解生成高级脂肪酸钠,该物质在饱和食盐水中溶解度较小,且密度小于水,则析出的肥皂浮在上层而不是沉于液面底部,C错误;油脂难溶于水,在乙醇中的溶解度较大,油脂制肥皂实验中加入一定量的乙醇为了增大油脂的溶解,增大与NaOH 溶液的接触面积,从而加快化学反应速率,D正确;正确选项D。

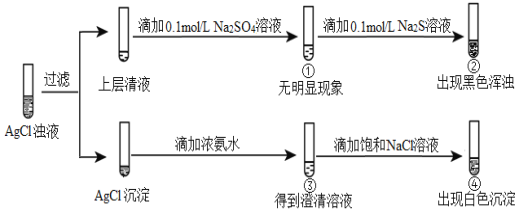
【题目】某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
装置 | 序号 | 试管中的药品 | 现象 |
持续通入
| 实验Ⅰ | 1.5 mL1 mol/L CuSO4溶液和3.5 mL 1mol/L NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
实验Ⅱ | 1.5 mL1 mol/L CuCl2溶液和3.5 mL 1 mol/L NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为__________________________________。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:__________________,检验Cu(OH)2洗涤干净的方法是____________________________________________。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3·H2O
=Cu(NH3)2++Cl-+2H2O、____________________________。
②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:

填写下表空格:
试剂1 | _________________ | 试剂2 | 蒸馏水 |
现象1 | _________________ | 现象2 | _________________ |
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:_________________。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,_________________________________,则说明砖红色沉淀是Cu2O。
【题目】柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:FeSO4+Na2CO3===FeCO3↓+Na2SO4 FeCO3 +C6H8O7=FeC6H6O7+CO2↑+H2O
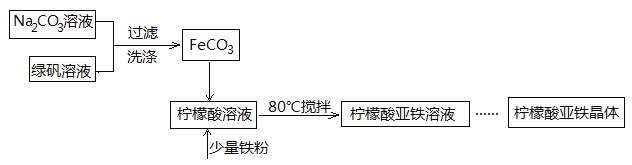
(1)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是____________________。
(2)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌反应。
①铁粉的作用是_________________。
②反应结束后,无需过滤,除去过量铁粉的方法是_____________。
(3)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是________________。
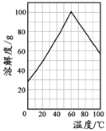
(4)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,先制备绿矾,再合成柠檬酸亚铁。请结合下图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):
①向一定量烧渣中加入足量的稀硫酸充分反应,过滤
②向滤液中滴加过量的NaOH溶液,过滤,充分洗涤固体
③向固体中加入足量稀硫酸至固体完全溶解
④再加入足量的铁粉,充分搅拌后,过滤得到FeSO4 溶液
⑤_______________________________________________,得到FeSO4·7H2O 晶体。
(5)取25.00g柠檬酸亚铁晶体(摩尔质量为246g/mol),配成100mL溶液,取20.00mL至锥形瓶中,另取0.2000mol.L-1的酸性KMnO4标准溶液装入酸式滴定管中,用氧化还原法测定柠檬酸亚铁晶体的质量分数,杂质不与酸性KMnO4标准溶液反应,经4次滴定,每次消耗KMnO4溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积 | 20.00mL | 19.98mL | 21.38mL | 20.02mL |
滴定终点时现象为:__________________________________柠檬酸亚铁的质量分数________________