��Ŀ����
����Ŀ��C��N��Si���γɶ��ָ�Ӳ�Ȳ��ϣ���Si3N4��C3N4��SiC��
��1�� Si3N4��C3N4��Ӳ�Ƚϸߵ���_________��������____________________��
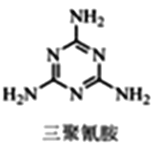
��2��C��N�ܺϳ������谷(��ͼ��ʾ)������Nԭ�ӵ��ӻ���ʽΪ________________��
��3��C��N�����γ�һ����Ԫ��״�л�������(im)����ṹΪ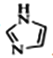 ��������[Co(im)6]SiF6�Ľṹʾ��ͼ��ͼ��ʾ:
��������[Co(im)6]SiF6�Ľṹʾ��ͼ��ͼ��ʾ:
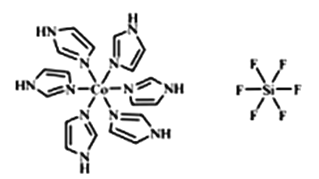
�ٻ�̬Coԭ�ӵĴ��������Ų�ʽΪ___________��N��Co2+֮��Ļ�ѧ��������_________________���жϵ�������__________________��
��������[SiF6]2-����ԭ��Si�ļ۲���Ӷ���Ϊ___________________��������[Co(im)6]2+��[SiF6]2-֮������������Ӽ�ľ�����������������������ã�����������ı�ʾʽ_______��(���磬ˮ������ı�ʾʽΪ: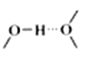 )��
)��
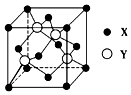
��4����-SiCΪ������ϵ���壬��������Ϊa����֪Siԭ�Ӱ뾶ΪrSi��Cԭ�Ӱ뾶ΪrC���þ�����ԭ�ӵķ�������Ϊ:
C:(0��0��0)��(1/2��1/2��0)��(1/2��0��1/2)��(0��1/2��1/2)������
Si:(1/4��1/4��1/4)��(1/4��3/4��3/4)��(3/4��1/4��3/4)��(3/4��3/4��1/4)��
����-SiC���������к���____��Siԭ�ӡ�___��Cԭ�����þ�����ԭ�ӵ����ռ��������İٷ���Ϊ______________(�г�����ʽ����)��
���𰸡� C3N4 ����ͬΪԭ�Ӿ��壬C��ԭ�Ӱ뾶С��Si����Si-N��ȣ�C-N�ļ����̣����ܴ� sp2 sp3 3s23p63d7 ��λ�� Nԭ���йµ��Ӷԣ�Co2+�пչ�� 6 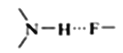 4 4 [16��(r3c+r3si)/(3a3)]��100%
4 4 [16��(r3c+r3si)/(3a3)]��100%
��������(1) Si3N4��C3N4��Ϊԭ�Ӿ��壬����Cԭ�Ӱ뾶С��Siԭ�ӣ�Si3N4�еĹ��ۼ��ļ�������C3N4�ļ�����Ӳ�Ƚϸߵ���C3N4���ʴ�Ϊ��C3N4������ͬΪԭ�Ӿ��壬C��ԭ�Ӱ뾶С��Si����Si-N��ȣ�C-N�ļ����̣����ܴ�
(2)���������谷�Ľṹ��֪��������Nԭ����2�֣�����һ������3��ԭ�ӣ�����һ���µ��Ӷԣ�����sp3�ӻ�����һ������2��ԭ�ӣ�����һ���µ��Ӷԣ�����sp2�ӻ����ʴ�Ϊ��sp2��sp3��
(3)��CoΪ27��Ԫ�أ���̬Coԭ�ӵ����Ų�ʽΪ1s22s22p63s23p63d74s2�����������Ų�ʽΪ3s23p63d7��Nԭ���йµ��Ӷԣ�Co2+�пչ��N��Co2+֮��Ļ�ѧ��Ϊ��λ�����ʴ�Ϊ��3s23p63d7����λ����Nԭ���йµ��Ӷԣ�Co2+�пչ����
��������[SiF6]2-����ԭ��Si�ļ۲���Ӷ���Ϊ6��������[Co(im)6]2+��[SiF6]2-֮������������Ӽ�ľ�����������F�ķǽ����Ժ�ǿ���ܹ���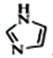 ��Nԭ���ϵ���ԭ���γ���������Ա�ʾΪ
��Nԭ���ϵ���ԭ���γ���������Ա�ʾΪ![]() ���ʴ�Ϊ��6��
���ʴ�Ϊ��6��![]() ��
��
(4)���ݾ�����ԭ�ӵķ��������֪��Cԭ��λ��������Ķ�������ģ�Siԭ��λ���������ڣ�������Χ��̼ԭ�ӹ�����������ṹ����-SiC���������к��е�Siԭ��Ϊ4�������е�Cԭ����=8��![]() +6��
+6��![]() =4�����������V1=a3��������̼ԭ�Ӻ�ԭ�ӵ������V2=
=4�����������V1=a3��������̼ԭ�Ӻ�ԭ�ӵ������V2=![]() ��(r3c+r3si)��4=
��(r3c+r3si)��4=![]() ��(r3c+r3si)��������ԭ�ӵ����ռ��������İٷ���=
��(r3c+r3si)��������ԭ�ӵ����ռ��������İٷ���=![]() ��100%=
��100%=![]() ��100%=
��100%=![]() ��100%���ʴ�Ϊ��4��4��
��100%���ʴ�Ϊ��4��4��![]() ��100%��
��100%��