题目内容
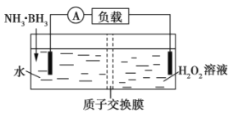
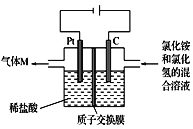
【题目】常温下,NCl3是一种黄色黏稠状液体,是制备新型水消毒剂ClO2的原料,可以采用如图所示装置制备NCl3。下列说法正确的是
A.每生成1 mol NCl3,理论上有4 mol H+经质子交换膜从右侧向左侧迁移
B.石墨极的电极反应式为NH4++3Cl--6e-==NCl3+4H+
C.可用湿润的淀粉-KI试纸检验气体M
D.电解过程中,质子交换膜右侧溶液的pH会减小
【答案】B
【解析】
由电池的正负极可判断,C电极为阳极,Pt电极为阴极。在C电极,发生反应NH4++3Cl--6e-==NCl3+4H+;在Pt电极,6H++6e-==3H2↑。
A.依据电荷守恒,在阳极区,每生成1 mol NCl3,理论上有6 mol H+经质子交换膜从右侧向左侧迁移,A不正确;
B.根据以上分析,在阳极(石墨极),NH4+失电子后生成的物质与Cl-作用生成NCl3,电极反应式为NH4++3Cl--6e-==NCl3+4H+,B正确;
C.气体M为H2,不能用湿润的淀粉-KI试纸检验,C不正确;
D.电解过程中,质子交换膜右侧溶液中每生成4molH+,将有6molH+通过质子交换膜向阴极区移动,所以pH会增大,D不正确;
故选B。

练习册系列答案
相关题目