题目内容
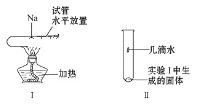
【题目】按照如图所示装置进行实验,填写有关现象及化学方程式。

(1)A中现象是___。
(2)B中浓硫酸的作用是___。
(3)C中发生反应的化学方程式为___。
(4)D中的现象是___,发生反应的离子方程式是___。
(5)E中收集的气体是___(填名称)。
【答案】试管口有无色液体生成 干燥CO2气体 2CO2+2Na2O2=2Na2CO3+O2 石灰水变浑浊 CO2+Ca2++2OH-=CaCO3↓+H2O 氧气
【解析】
(1)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;
(2)根据浓硫酸的性质分析;
(3)根据过氧化钠的性质分析;
(4)根据二氧化碳和石灰水的性质分析;
(5)根据反应后可能剩余的气体分析。
(1)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,则可观察到A中试管口有无色液体生成;
故答案为:试管口有无色液体生成;
(2)浓硫酸有吸水性,所以能作干燥剂,二氧化碳和浓硫酸不反应,所以能用浓硫酸干燥二氧化碳;
故答案为:干燥CO2气体;
(3)二氧化碳和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)二氧化碳能使澄清的石灰水变浑浊,所以未与过氧化钠反应的二氧化碳使石灰水变浑浊,发生反应的离子方程式为:CO2+Ca2++2OH-=CaCO3↓+H2O;
故答案为:石灰水变浑浊;CO2+Ca2++2OH-=CaCO3↓+H2O;
(5)碳酸氢钠分解生成的水蒸汽被浓硫酸吸收,未与过氧化钠反应的二氧化碳被石灰水吸收,所以剩余的气体就是二氧化碳和过氧化钠反应生成的氧气;
故答案为:氧气。

【题目】某研究性学习小组欲探究原电池的形成条件,按下图所示装置进行实验
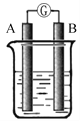
序号 | A | B | 烧杯中的液体 | 指针是否偏转 |
1 | Zn | Cu | 稀硫酸 | 有 |
2 | Zn | Zn | 稀硫酸 | 无 |
3 | Cu | C | 氯化钠溶液 | 有 |
4 | Mg | Al | 氢氧化钠溶液 | 有 |
分析上述数据,回答下列问题:
(1)实验1中电流由________极流向_______ 极(填“A”或“B”)
(2)实验4中电子由B极流向A极,表明负极是_________电极(填“镁”或“铝”)
(3)实验3 表明 ______
A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法不正确的是____________
A.相对活泼的金属一定做负极
B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的两种金属(或其中一种非金属)