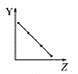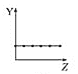题目内容
【题目】在25℃时,浓度均为0.5 mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的三种溶液,测得各溶液的c(NH4+)分别为a、b、c(单位为mol/L),下列判断正确的是
A.a=b=cB.a>b>cC.a>c>bD.c>a>b
【答案】D
【解析】
加入与原水解离子的水解性质相同的物质,对原水解离子有抑制作用,加入与原水解离子的水解性质相反的物质,对原水解离子有促进作用;三种溶液中均存在下述水解平衡:![]() ,对于(NH4)2CO3,因为
,对于(NH4)2CO3,因为![]() ,使
,使![]() 水解平衡向右移动,促进
水解平衡向右移动,促进![]() 水解.对于(NH4)2Fe(SO4)2,因为
水解.对于(NH4)2Fe(SO4)2,因为![]() ,因增大了c(H+),上述
,因增大了c(H+),上述![]() 水解平衡受到抑制,平衡向左移动,所以c>a>b,故答案为:D。
水解平衡受到抑制,平衡向左移动,所以c>a>b,故答案为:D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】CO2是一种常见的温室气体,它的吸收和利用也成为现代科技的热门课题。
(1)恒容密闭容器中,在Cu/ZnO催化剂作用下,可用CO2制备甲醇:CO2(g) + 3H2(g)CH3OH(g) + H2O(l) △H1,已知: CH3OH(g) +![]() O2(g)=CO2(g) + 2H2O(l) △H2,写出氢气燃烧热的热化学方程式________(△H用△H1、 △H2表示)。某温度下,在体积为2L的密闭容器中加入2mol CO2、5mol H2以及催化剂进行反应生成CH3OH 蒸气和水蒸气,达到平衡时H2的转化率是60%,其平衡常数为_______。
O2(g)=CO2(g) + 2H2O(l) △H2,写出氢气燃烧热的热化学方程式________(△H用△H1、 △H2表示)。某温度下,在体积为2L的密闭容器中加入2mol CO2、5mol H2以及催化剂进行反应生成CH3OH 蒸气和水蒸气,达到平衡时H2的转化率是60%,其平衡常数为_______。
(2)工业上用CO2催化加氢制取二甲醚:2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g)。在两个相同的恒容密闭容器中,充入等量的反应物,分别以Ir和Ce作催化剂,反应进行相同的时间后测得的CO2的转化率α(CO2)随反应温度的变化情况如图所示:
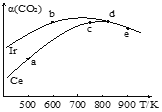
①用Ir和Ce作催化剂时,反应的活化能更低的是_________;
②a、b、c、d和e五种状态,反应一定达到平衡状态的是________,反应的ΔH ____0(填“>”、“=”或“<”);
③从状态a到c,CO2转化率不断增大的原因是__________;
④已知T℃下,将2 molCO2和6 molH2通入到体积为V L的密闭容器中进行上述反应,反应时间与容器内的总压强数据如表:
时间t/min | 0 | 10 | 20 | 30 | 40 |
总压强p/1000kPa | 1.0 | 0.83 | 0.68 | 0.60 | 0.60 |
该反应平衡时CO2的转化率为___________。
(3)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体CO2,得到NH4HCO3溶液,则反应NH4++HCO3-+H2ONH3·H2O+H2CO3的平衡常数K=_________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数Ka1=4×10-7,Ka2=4×10-11 )。