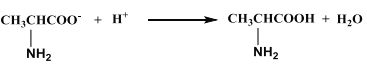
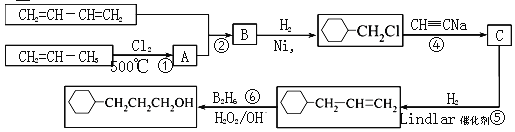
题目内容
【题目】由短周期元素或生活中常见的金属元素组成的中学常见无机物A、B、C、D、E、X存在如下图转化关系(部分生成物和反应条件略去)。下列推断不正确的是
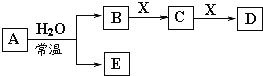
A. 若X是Na2CO3,C为一种温室气体,则A一定是氯气,且D和E不反应
B. 若A是单质,B和D的反应是![]() ,则E一定能还原Fe2O3
,则E一定能还原Fe2O3
C. 若D为CO,C能和E反应,则A一定为![]() ,其电子式
,其电子式![]()
D. 若C的溶液遇KSCN显红色,则A可能为氮的一种氧化物
【答案】A
【解析】
A、X是Na2CO3,C为CO2,当A为NO2,B为HNO3,E为NO,D为NaHCO3也符合转化关系,故A错误;B、根据B、D反应的离子方程式OH-+HCO3-═H2O+CO32-,A为活泼金属Na,B为NaOH、E为H2,X为CO2,C为Na2CO3,D为NaHCO3,H2在加热时能还原Fe2O3,故B正确;C、A为Na2O2,B为O2,E为NaOH,X为C,C为CO2,D为CO,符合转化关系,过氧化钠电子式为,![]() ,故C正确;D、若C的溶液遇KSCN显红色,说明C中含有铁离子,A可能为氮的一种氧化物,如二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮,B为硝酸,E为一氧化氮,硝酸与铁反应生成硝酸铁,则X为铁,D中含有亚铁离子,符合转化关系,故D正确;故选A。
,故C正确;D、若C的溶液遇KSCN显红色,说明C中含有铁离子,A可能为氮的一种氧化物,如二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮,B为硝酸,E为一氧化氮,硝酸与铁反应生成硝酸铁,则X为铁,D中含有亚铁离子,符合转化关系,故D正确;故选A。

 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成。B、C的组成元素相同,其化学式都可表示为Z2X2Y![]() ,且C的摩尔质量比B大80g/
,且C的摩尔质量比B大80g/![]() ,请回答:
,请回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为_________(填字母代号)
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)下表为B与F实验的部分内容:
①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
②向20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出B与稀H2SO4反应的离子方程式______________________;
写出②中反应方程式___________________________。
(3)现由6种粒子![]() (C中含有的阴离子)、
(C中含有的阴离子)、![]() 完成一个离子方程式,已知
完成一个离子方程式,已知![]() 为还原剂,则得到
为还原剂,则得到![]() 需氧化剂的物质的量为_______
需氧化剂的物质的量为_______![]() .
.
(4)化合物D和E相互转化D![]() E,若有D和
E,若有D和![]() 的混合物13.04g,加热到完全反应后,气体产物通过浓
的混合物13.04g,加热到完全反应后,气体产物通过浓![]() 增重3.42g,剩余气体通过碱石灰增生2.20g,则
增重3.42g,剩余气体通过碱石灰增生2.20g,则![]() 的化学式为__________________________.
的化学式为__________________________.