��Ŀ����
����Ŀ��ij��ѧ��ȤС���ͬѧͨ���������ϣ�����˲����һЩ��Ϣ���������±���
�ṹ��ʽ | HOOC-OOH |
�ܽ��� | ������ˮ���������Ҵ� |
���� | ��Լ��157������(175�����Ϸ����ֽ�) |
��ѧ���� | H2C2O4+Ca(OH)2=CaC2O4��+2H2O |
HOOC-COOH | |
2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4+10CO2��+8H2O |
��1������ͬѧ��ͨ��ʵ����֤�������ȷֽ�����е�CO2��CO(װ�÷���������Ҫ�������Լ���ѡ)��

����д���п��ڡ�
���� | A | B | C |
�����Լ� | ________ | ________ | NaOH��Һ |
�ڼ�������CO��ʵ�鷽����ʵ������__________________��
��2��ʵ���ҳ��ò����ƲⶨKMnO4��Һ��Ũ�ȡ�
��ȷ��ȡ2.680g�����ƣ�����ϡ�����ˮ�Ƴ�100.0 mL��Һ��ÿ��ȡ20.00mL��Һ����ƿ�У�������KMnO4��Һ����_______________(������ʽ��������ʽ��)�ζ����н��еζ����ظ������ζ��������Σ�ʵ��������±���ʾ������KMnO4��Һ�����ʵ���Ũ��Ϊ____________��
�ζ�ǰ��Ϊ | ��һ���յ� | �ڶ����յ� | �������յ� | |
�ζ���Һ��̶� | 0.00 mL | 20.02mL | 21.00mL | 19.98mL |
�ڽ�����KMnO4��Һ��H2C2O4��Һ��Ϻ��ֿ�ʼʱ��Һ��ɫ�����ԣ������ú�Ѹ����ɫ����Ը�ʵ������ijͬѧ��ΪKMnO4��Һ��H2C2O4��Һ�ķ�Ӧ�Ƿ��ȷ�Ӧ��������Һ�¶����ߣ���Ӧ���ʼӿ졣����뻹�п�����_____________��Ӱ�졣����ʵ��֤����IJ��룬��KMnO4��Һ��H2C2O4��Һ��ϡ�����⣬����Ҫѡ��ĺ����Լ���__________________��
���𰸡� �Ҵ� ����ʯ��ˮ ��C�������ܵ�ȼ���壬���Ƴ���ɫ������һ���ڱڸ��Ÿ�����ʯ��ˮ���ձ����ڻ����ϣ��ձ��ڱڵ�ʯ��ˮ����� ��ʽ 0.080 00 mol/L ����(��Mn2+�Ĵ�����) ������(�� MnSO4)
�������������������1����װ��AĿ���dz�ȥ���ᣬװ��B���ڼ��������̼���ݴ���ɱ��⣻
�ڸ���һ����̼ȼ�յĻ�����ɫ��ȼ�ղ��������̼��ɼ���һ����̼��
��2���ٸ��ݸ��������Һ����ǿ������ѡ��ʹ�õĵζ��ܣ����жϵζ����ݵ���Ч�ԣ�Ȼ���������ĵĸ��������Һ��ƽ����������ݷ�Ӧ2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O���ζ����ݼ��������KMnO4��Һ�����ʵ���Ũ�ȣ�
�ڸ��ݷ�Ӧ��ʼ������Ũ�Ƚ�С����Ӧ������������Ũ�������������ѡ���������ӵ��Լ�������֤��
��������1���ٸ����������ݿ�֪�������ܹ�ʹ����ʯ��ˮ����ǣ����ȹ����в�������������ɵĶ�����̼��һ����̼�к��в��ᣬ���������̼֮ǰ�������л��ܼ��Ҵ���ȥ���ᣬ����Aװ��Ϊ�Ҵ���Ȼ����װ��B����ʯ��ˮ���������̼���ڼ���һ����̼�ķ���Ϊ����C�������ܵ�ȼ���壬�������ɫ������һ���ڱڸ��ų���ʯ��ˮ���ձ����ڻ����ϣ��ձ��ڱڵ�ʯ��ˮ�������
��2���ٸ��������Һ����ǿ�����ԣ�Ӧ��ѡ����ʽ�ζ�����ȡ��
���ڵڶ��εζ��������ϴ�Ӧ�����������ĵĸ��������Һ��ƽ�����Ϊ![]() 20.00mL��
20.00mL��
2.680g�����Ƶ����ʵ���Ϊ�� ![]() =0.02mol��20mL��Һ�к��еĴ����Ƶ����ʵ���Ϊ��0.02mol��
=0.02mol��20mL��Һ�к��еĴ����Ƶ����ʵ���Ϊ��0.02mol��![]() =0.004mol�����ݷ�Ӧ����ʽ2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O��n��KMnO4��=
=0.004mol�����ݷ�Ӧ����ʽ2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O��n��KMnO4��=![]() n��H2C2O4��=
n��H2C2O4��=![]() n��Na2C2O4��=0.0016mol�����������Һ��Ũ��Ϊ��
n��Na2C2O4��=0.0016mol�����������Һ��Ũ��Ϊ�� ![]() =0.08000 mol/L����Ӱ�췴Ӧ���ʵ����س����¶ȣ����п���Ϊ������Ӱ�죬��Ӧ��������Ũ�������������ӿ������˴��������ã�ʹ��Ӧ���ʼӿ죻����ʵ��֤�����룬�����������Һ��������Һ��ϡ�����⣬����Ҫѡ���ܹ��ı�������Ũ�ȵ��Լ����������̡�
=0.08000 mol/L����Ӱ�췴Ӧ���ʵ����س����¶ȣ����п���Ϊ������Ӱ�죬��Ӧ��������Ũ�������������ӿ������˴��������ã�ʹ��Ӧ���ʼӿ죻����ʵ��֤�����룬�����������Һ��������Һ��ϡ�����⣬����Ҫѡ���ܹ��ı�������Ũ�ȵ��Լ����������̡�

 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
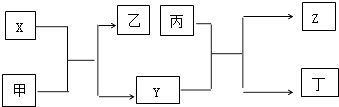
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�����Ŀ�����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ�����ԭ��������XYTZ��������
Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
X | �����������Ǵ�����������2�� |
Y | �����µ���Ϊ˫ԭ�ӷ��ӣ����⻯��ˮ��Һ�ʼ��� |
T | �����������ǵ��Ӳ�����2�� |
Z | Ԫ�����������+7�� |
��1������Ԫ��ԭ�Ӱ뾶�ɴ�С��˳���ǣ�дԪ�ط��ţ� ��
��2��Ԫ��Y����Ԫ���γɵ�һ������YH4+ �� д�������ĵ���ʽ����Ԫ�ط��ű�ʾ����
��3��TԪ�صļ������ӵĽṹʾ��ͼ�� ��
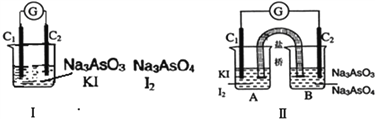
��4��֤�������ӵĻ�ԭ�Ա�Z��ǿ�����ӷ���ʽ�� ��
��5��Ԫ��Z�ĵ���������������Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��6����9g����X������������ȼ�գ���������ͨ��1L 1molL��1NaOH��Һ�У���ȫ���պ���Һ�ڼ�ѹ�������������ɣ��õ������ᾧˮ�Ĺ�������Ϊg��