题目内容
1.在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表.下列判断不正确的是( ) | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | a=6.00 | |
| B. | 同时改变反应温度和蔗糖的浓度,v可能不变 | |
| C. | b<318.2 | |
| D. | 不同温度时,蔗糖浓度减少一半所需的时间相同 |
分析 A、由表可知温度由318.2→328.2℃,在浓度相同的情况下$\frac{{v}_{318.2}}{{v}_{328.2}}$=0.4,由此解答;
B、由表可知温度由318.2℃→b,浓度由0.3mol/L→0.5mol/L,速率相等;
C、由表可知温度由328.2℃→b,在浓度相同的情况下,水解速率变小,所以温度降低;
D、温度越高反应速率越快,所以蔗糖浓度减少一半所需的时间不同,温度高的所需时间短.
解答 解:A、由表可知温度由318.2→328.2℃,在浓度相同的情况下$\frac{{v}_{318.2}}{{v}_{328.2}}$=0.4,所以a=$\frac{2.4}{0.4}$=6,故A正确;
B、由表可知温度由318.2℃→b,浓度由0.3mol/L→0.5mol/L,速率相等,都是1.80,所以v可能不变,故B正确;
C、由表可知温度由328.2℃→b,在浓度相同的情况下,水解速率变小,所以温度降低,所以温度b<318.2,故C正确;
D、温度越高反应速率越快,所以蔗糖浓度减少一半所需的时间不同,温度高的所需时间短,故D错误;
故选D.
点评 本题考查较综合,涉及反应速率计算、影晌速率的因素分析等,侧重学生表格数据分析及计算能力的考查,注重对高考高频考点的训练,题目难度中等.

练习册系列答案
相关题目
11.下列离子在水溶液中一定能大量共存的是( )
| A. | Fe3+、NO${\;}_{3}^{-}$、SCN-、CO${\;}_{3}^{2-}$ | B. | Fe2+、H+、Cl-、ClO- | ||
| C. | Mg2+、Na+、CH3COO-、SO${\;}_{4}^{2-}$ | D. | Na+、AlO${\;}_{2}^{-}$、Cl-、HCO${\;}_{3}^{-}$ |
12.合成导电高分子材料PPV的反应:
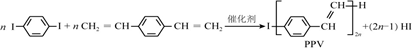
下列说法正确的是( )
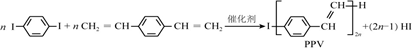
下列说法正确的是( )
| A. | 合成PPV的反应为加聚反应 | |
| B. | PPV与聚苯乙烯具有相同的重复结构单元 | |
| C. |  和苯乙烯互为同系物 和苯乙烯互为同系物 | |
| D. | 通过质谱法测定PPV的平均相对分子质量,可得其聚合度 |
9.下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是( )
| A. |  观察Fe(OH)2的生成 观察Fe(OH)2的生成 | |
| B. |  配制一定物质的量浓度的NaNO3溶液 配制一定物质的量浓度的NaNO3溶液 | |
| C. |  实验室制取氨 实验室制取氨 | |
| D. |  验证乙烯的生成 验证乙烯的生成 |
16.下列制作铅笔的材料与相应工业不对应的是( )
| A. | 橡皮擦--橡胶工业 | B. | 铝合金片--冶金工业 | ||
| C. | 铅笔芯--电镀工业 | D. | 铅笔漆--涂料工业 |
6.下列说法不正确的是( )
| A. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 | |
| B. | 在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物(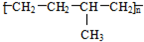 )可由单体CH3CH=CH2和CH2=CH2加聚制得 )可由单体CH3CH=CH2和CH2=CH2加聚制得 |
13.进行化学实验时应强化安全意识.下列做法正确的是( )
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 制备乙烯时向乙醇和浓硫酸的混合液中加入碎瓷片 |
8. 为探究FeCl2溶液电解时阴阳极的产物,某兴趣小组用如下装置进行实验:
为探究FeCl2溶液电解时阴阳极的产物,某兴趣小组用如下装置进行实验:
(査阅资料:电解能否发生、电极反应及其速率,与电压大小、离子浓度等因素有关)
I.电极a表面始终未出现气泡,但产生了银灰色有金属光泽的固体,该电极的电极反应式为:Fe2++2e-=Fe
Ⅱ.电极b开始一段时间内,表面无气泡产生,周围液体出现红褐色,逐渐浑浊.吸取该电极周围少许液体于两支试管中,一支试管中滴入淀粉一KI溶液,液体颜色不变;另一支试管中先加盐酸酸化,再滴入KSCN溶液,巧液变为红色.
结论:电解过程中产生了Fe3+,同时水解产生了红褐色物质.
(1)加盐酸酸化时发生的反应是Fe(OH)3+3H+=Fe3++3H2O(用离子方程式表示)
(2)对电解过程中Fe3+产生的原因进行猜想:
猜想①:Cl-在阳极放电,生成的Cl2将Fe2+氧化成Fe3%
猜想②:Fe2+在阳极直接放电生成Fe3+
猜想③:…
(3)设计实验验证猜想①
供选择的试剂:1mol/LFeS04溶液、lmoi/L 盐酸、2mol/L 盐酸、lmol/LNaCl 溶液、2moJ/L NaCl溶液、淀粉一KI溶液、KSCN溶液,蒸馏水
 为探究FeCl2溶液电解时阴阳极的产物,某兴趣小组用如下装置进行实验:
为探究FeCl2溶液电解时阴阳极的产物,某兴趣小组用如下装置进行实验:(査阅资料:电解能否发生、电极反应及其速率,与电压大小、离子浓度等因素有关)
I.电极a表面始终未出现气泡,但产生了银灰色有金属光泽的固体,该电极的电极反应式为:Fe2++2e-=Fe
Ⅱ.电极b开始一段时间内,表面无气泡产生,周围液体出现红褐色,逐渐浑浊.吸取该电极周围少许液体于两支试管中,一支试管中滴入淀粉一KI溶液,液体颜色不变;另一支试管中先加盐酸酸化,再滴入KSCN溶液,巧液变为红色.
结论:电解过程中产生了Fe3+,同时水解产生了红褐色物质.
(1)加盐酸酸化时发生的反应是Fe(OH)3+3H+=Fe3++3H2O(用离子方程式表示)
(2)对电解过程中Fe3+产生的原因进行猜想:
猜想①:Cl-在阳极放电,生成的Cl2将Fe2+氧化成Fe3%
猜想②:Fe2+在阳极直接放电生成Fe3+
猜想③:…
(3)设计实验验证猜想①
供选择的试剂:1mol/LFeS04溶液、lmoi/L 盐酸、2mol/L 盐酸、lmol/LNaCl 溶液、2moJ/L NaCl溶液、淀粉一KI溶液、KSCN溶液,蒸馏水
| 操作 | 现象和结论 |
| ①取-定量2mol/L NaCl溶液,调 节溶液pH为4.91:再以相间装置进行电解. ②电解相同时间后,若电极b表面无气泡,取少量阳极附近的溶液,滴入淀粉KI溶液 | |

 溶液出现蓝色且30s内不褪色
溶液出现蓝色且30s内不褪色