题目内容
13.已知A为淡黄色固体,T、R 为两种常见的用途广泛的金属单质,D具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体.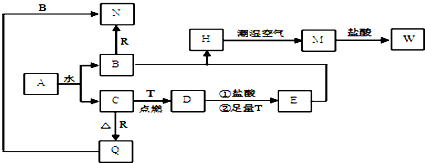
(1)写出下列物质的化学式:D:Fe3O4 R:Al.写出A的电子式

(2)按要求写出下列反应方程式:
H在潮湿空气中变为M的化学方程式4 Fe(OH)2+O2+2H2O═4 Fe(OH)3
B与R反应的化学方程式2Al+2OH-+2H2O═2AlO2-+3H2↑
D与盐酸反应的离子方程式Fe3O4+8H+═Fe2++2Fe3++4H2O
(3)向沸水中加入W饱和溶液,可制得一种红褐色透明液,该反应的离子方程式Fe3++3H2O=Fe(OH)3(胶体)+3H+.
分析 A为淡黄色固体,且A能和水反应,则A是Na2O2,A和水反应生成NaOH和O2,C是无色无味的气体,则C是O2、B是NaOH;D是具有磁性的黑色晶体,则D是Fe3O4,Fe在氧气中燃烧生成四氧化三铁,则T是Fe,R和氧气反应生成氧化物Q,Q能和NaOH溶液反应,则Q是Al2O3、R是Al,N是NaAlO2,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M,则H是Fe(OH)2、M是Fe(OH)3,Fe3O4和HCl、Fe反应后得到E,E为FeCl2,Fe(OH)3和HCl反应生成W,则W是FeCl3,再结合问题分析解答.
解答 解:A为淡黄色固体,且A能和水反应,则A是Na2O2,A和水反应生成NaOH和O2,C是无色无味的气体,则C是O2、B是NaOH;D是具有磁性的黑色晶体,则D是Fe3O4,Fe在氧气中燃烧生成四氧化三铁,则T是Fe,R和氧气反应生成氧化物Q,Q能和NaOH溶液反应,则Q是Al2O3、R是Al,N是NaAlO2,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M,则H是Fe(OH)2、M是Fe(OH)3,Fe3O4和HCl、Fe反应后得到E,E为FeCl2,Fe(OH)3和HCl反应生成W,则W是FeCl3,
(1)通过以上分析知,D、R分别是Fe3O4、Al,A是Na2O2,电子式为 ,
,
故答案为:Fe3O4;Al; ;
;
(2)H是Fe(OH)2,Fe(OH)2不稳定,易被空气氧化生成Fe(OH)3,反应方程式为4 Fe(OH)2+O2+2H2O═4 Fe(OH)3,铝和NaOH溶液反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,四氧化三铁和稀盐酸反应生成氯化铁、氯化亚铁和水,离子反应方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O,
故答案为:4 Fe(OH)2+O2+2H2O═4 Fe(OH)3;2Al+2OH-+2H2O═2AlO2-+3H2↑;Fe3O4+8H+═Fe2++2Fe3++4H2O;
(3)向沸水中加入FeCl3饱和溶液,可制得一种红褐色液体,该液体是氢氧化铁胶体,反应的离子方程式为Fe3++3H2O=Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O=Fe(OH)3(胶体)+3H+.
点评 本题以Na、Al、Fe及其化合物为载体考查了金属元素及其化合物的推断,根据H的颜色变化、A的颜色及性质、D的性质为突破口采用正逆结合的方法进行推断,熟悉物质性质是解本题关键,再结合物质间的转化来解答,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | mol | B. | g/mol | C. | g | D. | mol/L |
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将铁片放入浓硫酸中 | 无明显变化 | 铁与浓硫酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | 乙醇中的氢原子均能与Na反应 |
| D | 氯气通入品红溶液中 | 品红褪色 | 氯分子有漂白作用 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 45% | B. | 50% | C. | 37.5% | D. | 65% |
| A. | 将SO2通入BaCl2 溶液中至饱和,无沉淀产生,再通入Cl2,产生白色沉淀 | |
| B. | 纯锌与稀硫酸反应产生氢气速率较慢;再加入少量CuSO4 固体,速率不改变 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉可以溶解 | |
| D. | 向AlCl3 溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4 溶液,沉淀消失 |
| A. | 1 mol ${\;}_{8}^{16}$OD-离子含有的质子、中子数均为10NA | |
| B. | 标准状况下,4.48 L己烷含有的分子数为0.2NA | |
| C. | 含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | |
| D. | VL a mol•L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目等于3NA |
| A. | 将40g NaOH溶解于1L水中配成的NaOH溶液 | |
| B. | 常温常压下将22.4L HCl 气体溶于水配成1L的盐酸溶液 | |
| C. | 将100mL 10mol/L的浓盐酸加水900mL混合所配成的溶液 | |
| D. | 从1000mL 1mol/L NaCl溶液中取出100mL的溶液 |
| A. | SiO2是酸性氧化物,它不溶于水也不溶于任何酸 | |
| B. | 木材浸过水玻璃后,具有防腐蚀性能且不易着火 | |
| C. | 因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强 | |
| D. | 氯气泄漏后,人应逆风且往低处跑 |