题目内容
10.今有A、B、C、D、E、F六种装置,如图所示.(胶塞、导管可自由选用)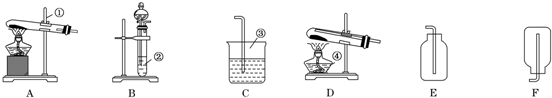
(1)写出①~④的仪器名称:①铁架台,②试管,③烧杯,④酒精灯.
(2)实验室制取并收集氧气时应选择A和E相连接,制取并收集氢气时应选择B和F相连接.
(3)做木炭还原氧化铜并检验生成气体的实验,应选择D和C相连接,检验气体时观察到的实验现象是澄清石灰水变浑浊.
(4)制取氢气并做还原氧化铜的实验,应选择B和D装置,实验结束时应先停止加热,待试管冷却后,再停止通氢气,其原因是防止铜被氧化.
分析 (1)根据仪器的图形、构造判断仪器的名称;
(2)实验室可用加热高锰酸钾固体制备氧气,用稀硫酸和锌反应制备氢气,氢气密度比空气小,可用向下排空法收集氢气;
(3)做木炭还原氧化铜并检验生成气体的实验,可在大试管中加热条件下进行,用澄清石灰水检验;
(4)用稀硫酸和锌反应制备氢气,在大试管中加热条件下进行还原实验,实验结束时应先停止加热,待试管冷却后,再停止通氢气,防止铜被氧化.
解答 解:(1)由仪器的图形、构造判断①~④的仪器名称分别为铁架台、试管、烧杯、酒精灯,故答案为:铁架台;试管;烧杯;酒精灯;
(2)实验室可用加热高锰酸钾固体制备氧气,氧气密度比空气大,可用向上排空法收集,则选用A、E装置,用稀硫酸和锌反应制备氢气,氢气密度比空气小,可用向下排空法收集氢气,则选用B、F装置,故答案为:A;E;B;F;
(3)做木炭还原氧化铜并检验生成气体的实验,可在大试管中加热条件下进行,用澄清石灰水检验,可用D、C装置,可观察到澄清石灰水变浑浊,故答案为:D、C;澄清石灰水变浑浊;
(4)用稀硫酸和锌反应制备氢气,在大试管中加热条件下进行还原实验,可用B、D装置,实验结束时应先停止加热,待试管冷却后,再停止通氢气,防止铜被氧化.
故答案为:B;D;防止铜被氧化.
点评 本题主要考查物质的制备以及性质检验,为高频考点,侧重于学生的分析、实验能力的考查,要想解答好这类题目,就要熟记常用气体的发生装置和收集装置与选取方法及其依据,还有氧气、二氧化碳的实验室制取方法,有时还需弄清图示信息等等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.关于下列各实验装置图的叙述中,正确的是( )

| A. | 装置①可用于分离碘和氯化钠的固体混合物 | |
| B. | 装置②可用于吸收HCl或NH3气体 | |
| C. | 装置③可用于分解NH4HCO3制备NH3 | |
| D. | 装置④b口进气可收集CO2或NO气体 |
1.质量分数为18% 的乙醇溶液和质量分数为72%的乙醇溶液等体积混合,混合后的质量分数可能为( )
| A. | 45% | B. | 50% | C. | 37.5% | D. | 65% |
5.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1 mol ${\;}_{8}^{16}$OD-离子含有的质子、中子数均为10NA | |
| B. | 标准状况下,4.48 L己烷含有的分子数为0.2NA | |
| C. | 含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | |
| D. | VL a mol•L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目等于3NA |
15.已知Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,则下列关于该反应的叙述不正确的是( )
| A. | 该反应中旧键断裂需吸收能量小于新键形成需放出能量 | |
| B. | 上述热化学方程式中的△H的值与反应物的用量无关 | |
| C. | 该反应的化学能可以转化为电能 | |
| D. | 反应物的总能量高于生成物的总能量 |
2.下列溶液中溶质的物质的量浓度为1mol•L-1的是( )
| A. | 将40g NaOH溶解于1L水中配成的NaOH溶液 | |
| B. | 常温常压下将22.4L HCl 气体溶于水配成1L的盐酸溶液 | |
| C. | 将100mL 10mol/L的浓盐酸加水900mL混合所配成的溶液 | |
| D. | 从1000mL 1mol/L NaCl溶液中取出100mL的溶液 |
19.化学与生活息息相关,下列说法正确的是( )
| A. | 氧化钙和铁粉常用作食品干燥剂 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| C. | 碳酸钡不溶于水因此在医疗上用作钡餐 | |
| D. | “血液透析”利用了胶体的性质 |
20.下列化合物分子中所有原子一定处于同一平面的是( )
| A. | 甲苯 | B. | 1-丁烯 | C. | 溴苯 | D. | 丙烯 |