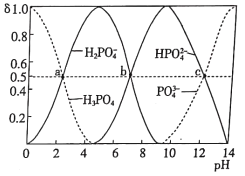
题目内容
【题目】公认的人体必需金属元素是钠和钾。在动物中,钠主要是以氯化钠形式存在于细胞外液中,依靠氯化钠可以把一定量的水吸到细胞里来,使细胞里维持一定的水分。某试剂瓶上贴有如下标签,对该试剂理解正确的是 ( )
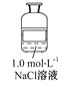
A.该溶液中含有的微粒主要有NaCl、Na+、Cl-、H2O
B.若取50毫升溶液,其中的c(Cl-)=0.05 mol·L-1
C.若取该溶液与100 mL 0.1 mol·L-1AgNO3溶液完全反应,需要取该溶液10 mL
D.该溶液与1.0 mol·L-1Na2SO4溶液的c(Na+)相等
【答案】C
【解析】
A.NaCl在溶液中完全电离出钠离子和氯离子,在溶液中不存在NaCl分子,故A错误;
B.若取50毫升溶液,取出溶液浓度不变,则c(Cl-)=c(NaCl)=1.0mol/L,故B错误;
C.100mL 0.1mol/LAgNO3溶液中:n(AgNO3)=0.1mol/L×0.1L=0.01mol,则需要n(NaCl)=n(AgNO3)=0.01mol,需要该NaCl溶液的体积为:![]() =0.01L=10mL,故C正确;
=0.01L=10mL,故C正确;
D.1.0mol/LNaCl溶液中c(Na+)=1.0mol/L,1.0mol/LNa2SO4溶液中c(Na+)=1.0mol/L×2=2.0mol/L,故D错误;
故答案为C。

 名校课堂系列答案
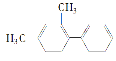
名校课堂系列答案【题目】丙烯(C2H6)是石油化工行业重要的有机原料之一,主要用于生产聚丙烯、二氯丙烷、异丙醇等产品。
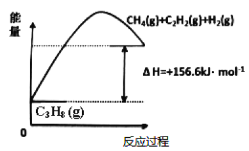
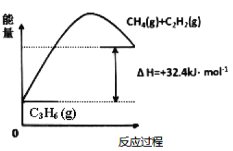
(1)丙烷脱氢制备丙烯。由图可得C3H8(g)C3H6(g)+H2(g) H=____________kJ/mol
①为了同时提高反应速率和反应物的平衡转化率,可采取的措施是________。
②目前在丙烷脱氢制丙烯时常通入适量的O2,让其同时发生下列反应:2C3H8(g) +O2(g)2C3H6(g)+2H2O(g) H=-235kJ/mol,通入O2的目的是_______。
(2)以C4H8和C2H4为原料发生烯烃歧化反应C4H8(g)+C2H4(g)2C3H6(g) H>0
①某温度下,上述反应中,正反应速率为v正=K正c(C4H8)c(C2H4)、逆反应速率为v逆=K逆c2(C3H6),其中K正、K逆为速率常数,该反应使用WO3/SiO2为催化剂,下列说法中正确的是_____________
A.催化剂参与了歧化反应,但不改变反应历程
B.催化剂使K正和K逆增大相同的倍数
C.催化剂降低了烯烃歧化反应的活化能,增大了活化分子百分数
D.速率常数的大小与反应程度无关系
②已知t1min时达到平衡状态,测得此时容器中n(C4H8)=amol,n(C2H4)=2amol,n(C3H6)=bmol,且平衡时C3H6的体积分数为25%。再往容器内通入等物质的量的C4H8和C2H4,在新平衡中C3H6的体积分数___________25%(填“>”、“<”、“=”)。
(3)工业上可用丙烯加成法制备1,2-二氯丙烷(CH2ClCHClCH3),主要副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
Ⅰ. CH2=CHCH3(g)+Cl2(g)CH2ClCHClCH3(g)
II. CH2=CHCH3(g)+Cl2(g)CH2=CHCH2Cl(g)+HCl(g)
一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g)。在催化剂作用下发生反应Ⅰ,容器内气体的压强随时间的变化如表所示。
时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 80 | 74.2 | 69.2 | 65.2 | 61.6 | 57.6 | 57.6 |
①用单位时间内气体分压的变化来表示反应速率,即![]() ,则前120min内平均反应速率v(CH2ClCHClCH3)=____________kPamin-1。
,则前120min内平均反应速率v(CH2ClCHClCH3)=____________kPamin-1。
②该温度下,若平衡时HCl的体积分数为12.5%,反应Ⅰ的平衡常数Kp=__________kPa-1(Kp为以分压表示的平衡常数,保留小数点后2位)。