题目内容
【题目】H2S2O3是一种弱酸,实验室欲用0.01mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,下列说法合理的是( )
A.该滴定可用甲基橙作指示剂
B.Na2S2O3是该反应的还原剂
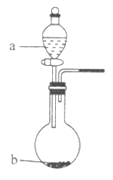
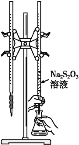
C.该滴定可选用如图所示装置
D.该反应中每生成1molNaI,电子转移数为2NA
【答案】B
【解析】
A、溶液中有单质碘,加入淀粉溶液呈蓝色,碘与亚硫酸钠发生氧化还原反应,当反应终点时,单质碘消失,蓝色褪去,应加入淀粉溶液作指示剂,故A错误;
B、Na2S2O3中S元素化合价升高,被氧化,该物质作还原剂,故B正确;
C、Na2S2O3溶液显碱性,应该用碱式滴定管,故C错误;
D、I2+2Na2S2O3=2NaI+Na2S4O6,反应中每消耗2mol Na2S2O3,电子转移数为2mol,每生成1molNaI,电子转移数为1NA,故D错误;
故选B。

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目