��Ŀ����
����Ŀ���������ܼ��㷺�������͵��¡�ú���ܡ���ˮ���ġ�Ь�ϡ����ڸ�װ��Ʒ�����������͵�������Ʒ�ȡ��������ܼ�G��ijҽҩ�м���N��һ�ֺϳ�·�����£����ַ�Ӧ������ȥ����

��֪��
��1��
��2��CH3CH=CHCH2CH3![]() CH3COOH+CH3CH2COOH
CH3COOH+CH3CH2COOH
��ش��������⣺
��1��N�й����ŵ�����Ϊ________����Ӧ�ڵ��Լ��������ǣ�__________��
��2����Ӧ�ݵķ�Ӧ������________����Ӧ��ķ�Ӧ������____________��
��3��I�Ľṹ��ʽΪ____________��
��4��д��B��H��Ӧ���ɾ������ܼ�G�Ļ�ѧ����ʽ__________��
��5��H��ͬ���칹���������������Ĺ���______�֣����������칹��
��1mol����������2molNaOH��Һ��Ӧ
��1mol��������������Һ��Ӧ����4molAg
������ֻ��2����
���к˴Ź���������ʾλ��壬�ҷ������Ϊ3��1��2����________��д��һ�ֽṹ��ʽ��
��6���ο����Ϻϳ�·�ߵ���Ϣ�����һ���Ա�������Ҵ�Ϊԭ�Ϻϳ�![]() ��·�ߣ����Լ���ѡ����ע����Ӧ��������_________��
��·�ߣ����Լ���ѡ����ע����Ӧ��������_________��
ʾ����ԭ��![]() ������
������
���𰸡� �ʻ������� �������Ƶ�ˮ��Һ������ ��ȥ��Ӧ ȡ����Ӧ (CH3)2CHOH  11 (HCOO)2C(CH2CH3)2 , (HCOOCH2)2C(CH3)2 ����дһ�֣�
11 (HCOO)2C(CH2CH3)2 , (HCOOCH2)2C(CH3)2 ����дһ�֣� 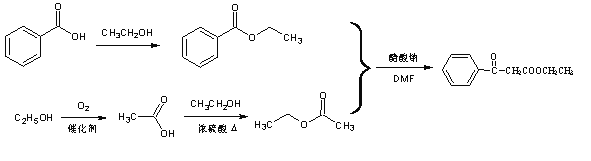
����������1������N�Ľṹ��ʽ��֪N�й����ŵ�����Ϊ�ʻ�����������ϩ����ӳ�����A��A��CH2BrCH2Br��Aˮ������BΪ�Ҷ�������˷�Ӧ�ڵ��Լ����������������Ƶ�ˮ��Һ�����ȣ���2��������C����Է���������92�����C�Ǽױ������巢��ȡ����Ӧ����D��D�����������ӳɷ�Ӧ����E��F��������H��������֪��Ϣ��֪H�Ľṹ��ʽΪ![]() ����˵��E����F����ȥ��Ӧ����D��E�Ľṹ��ʽΪ
����˵��E����F����ȥ��Ӧ����D��E�Ľṹ��ʽΪ ��
�� �����Է�Ӧ�ݵķ�Ӧ��������ȥ��Ӧ��������֪��Ϣ���N��H�Ľṹ��ʽ��֪I�Ľṹ��ʽΪ(CH3)2CHOH��M�Ľṹ��ʽΪ(CH3)2CHOOCCH2CH(CH3)CH2CH2COOCH(CH3)2����Ӧ��ķ�Ӧ������ȡ����Ӧ����3���������Ϸ�����֪I�Ľṹ��ʽΪ(CH3)2CHOH����4��B��H��Ӧ���ɾ������ܼ�G�Ļ�ѧ����ʽΪ
�����Է�Ӧ�ݵķ�Ӧ��������ȥ��Ӧ��������֪��Ϣ���N��H�Ľṹ��ʽ��֪I�Ľṹ��ʽΪ(CH3)2CHOH��M�Ľṹ��ʽΪ(CH3)2CHOOCCH2CH(CH3)CH2CH2COOCH(CH3)2����Ӧ��ķ�Ӧ������ȡ����Ӧ����3���������Ϸ�����֪I�Ľṹ��ʽΪ(CH3)2CHOH����4��B��H��Ӧ���ɾ������ܼ�G�Ļ�ѧ����ʽΪ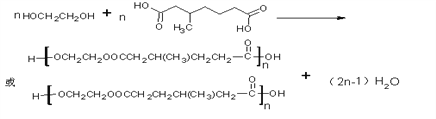 ����5����1mol����������2molNaOH��Һ��Ӧ����1mol��������������Һ��Ӧ����4molAg��˵������2�������γɵ�������������ֻ��2�������������������л���ṹ��ʽΪ�����HCOO-C-C-C-OOCH�������������������ڡ�������ԣ�����5�֣������HCOO-C-C-OOCH�������Ǽ����һ���ֻ�������ڻ���ԡ������HCOO-C-OOCH���������2���һ���֧���������������CH(CH3)CH2CH3�����ǣ�CHCH(CH3)2��������11�֡����к˴Ź���������ʾλ��壬�ҷ������Ϊ3��1��2����(HCOO)2C(CH2CH3)2 ��(HCOOCH2)2C(CH3)2����6���ο����Ϻϳ�·�ߵ���Ϣ���Ա�������Ҵ�Ϊԭ�Ϻϳ�
����5����1mol����������2molNaOH��Һ��Ӧ����1mol��������������Һ��Ӧ����4molAg��˵������2�������γɵ�������������ֻ��2�������������������л���ṹ��ʽΪ�����HCOO-C-C-C-OOCH�������������������ڡ�������ԣ�����5�֣������HCOO-C-C-OOCH�������Ǽ����һ���ֻ�������ڻ���ԡ������HCOO-C-OOCH���������2���һ���֧���������������CH(CH3)CH2CH3�����ǣ�CHCH(CH3)2��������11�֡����к˴Ź���������ʾλ��壬�ҷ������Ϊ3��1��2����(HCOO)2C(CH2CH3)2 ��(HCOOCH2)2C(CH3)2����6���ο����Ϻϳ�·�ߵ���Ϣ���Ա�������Ҵ�Ϊԭ�Ϻϳ�![]() ��·��ͼΪ
��·��ͼΪ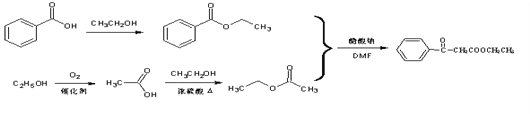 ��
��