题目内容
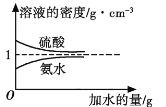
【题目】已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶质的物质的量浓度/mol·L1 | 溶液的密度/g·cm3 | |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为 (不写单位,用含c1、 ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为 mol·L1。
(3)将物质的量浓度分别为c2 mol·L1和![]() c2 mol·L1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm3,所得溶液的物质的量浓度
c2 mol·L1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm3,所得溶液的物质的量浓度 ![]() c2 mol·L1(设混合后溶液的体积变化忽略不计)。
c2 mol·L1(设混合后溶液的体积变化忽略不计)。
【答案】
(1)![]() %
%
(2)c1 /2
(3)大于 大于
【解析】
(1)设硫酸的体积为1 L,则w(H2SO4)= ![]() ×100%=
×100%=![]() %。
%。
(2)硫酸与水等体积混合(混合后溶液的体积变化忽略不计),溶液的体积变为原来的2倍,则浓度为c1/2
mol·L1。
(3)根据图像可知,氨水的浓度越大,密度越小,则c2 mol·L1氨水的密度小于![]() c2 mol·L1氨水的密度,等质量时,
c2 mol·L1氨水的密度,等质量时,![]() c2 mol·L1氨水的体积小于c2 mol·L1氨水的体积。两者混合后,所得溶液的密度一定比ρ2大,所得溶液的物质的量浓度趋近于体积大者,故大于
c2 mol·L1氨水的体积小于c2 mol·L1氨水的体积。两者混合后,所得溶液的密度一定比ρ2大,所得溶液的物质的量浓度趋近于体积大者,故大于![]() c2 mol·L1。
c2 mol·L1。

【题目】实验是化学研究的重要方法之一,某同学为了制备氯气并探究氯气等物质的相关性质,设计如图所示的实验方案:
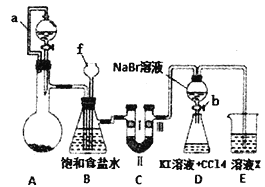
(1)仪器f的名称___________。
(2)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr207),还原产物是CrCl3,写出A中离子方程式:________________________________。
(3)B装置的作用除了用来除去氯气中的氯化氢外还有____________。
(4)装置C的作用是探究有氧化性的物质是否一定有漂白性,下列最佳试剂组合是______________
(填序号)
① | ② | ③ | ④ | |
I | 湿润的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 湿润的红纸条 |
II | 碱石灰 | 浓硫酸 | 硅胶 | 氯化钠 |
II! | 干燥的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 干燥的红纸条 |
(5)利用D装置证明溴的非金属性比碘强的实验操作是:实验完毕,_______,振荡锥形瓶,现象是 _____________________________________________。(补充完整上述实验操作和现象)
(6)D装置进行实验时存在的明显不足是________________________________。