题目内容
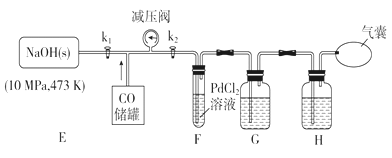
【题目】一种浓差电池如图所示,阴、阳离子交换膜交替放置,中间的间隔交替充以河水和海水,选择性透过Cl和Na+,在两电极板形成电势差,进而在外部产生电流。下列关于该电池的说法正确的是( )
A.a电极为电池的正极,电极反应为2H++2e═H2↑
B.C为阴离子交换膜,A为阳离子交换膜
C.负极隔室的电中性溶液通过阳极表面的还原作用维持
D.该电池的缺点是离子交换膜价格昂贵,优点是电极产物有经济价值
【答案】AD
【解析】
A. b电极电子流出,b为电池的负极,a电极为电池的正极,电极反应为2H++2e═H2↑,A项正确;
B. 钠离子向a电极方向移动,氯离子向b电极方向移动,所以A为阴离子交换膜,C为阳离子交换膜,B项错误;
C. 负极隔室中氯离子失去电子产生氯气,保持溶液中的电荷守恒,C项错误;
D. 离子交换膜价格昂贵,电极产物有氢气,是很好的清洁能源,氯气是重要的化工原料,经济价值是非常高的,D项正确;
答案选AD。

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目