题目内容
【题目】如图为锌铜原电池示意图,下列说法错误的是( )
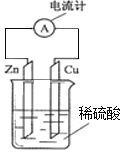
A.锌片为负极,且锌片逐渐溶解
B.电子由锌片通过导线流向铜片
C.铜为正极,铜不易失电子而受到保护
D.溶液中阳离子向![]() 极移动,且
极移动,且![]() 极上发生的是氧化反应
极上发生的是氧化反应
【答案】D
【解析】
由图中的铜锌原电池可知,Zn活泼,则Zn作负极,Cu作正极,发生电池反应为Zn+H2SO4═ZnSO4+H2↑,电子由负极流向正极,该装置将化学能转变为电能,以此来解答。
A.Zn作负极,则Zn失去电子发生氧化反应,锌片逐渐溶解,故A正确;
B.Zn作负极,Cu作正极,则电子由锌片通过导线流向铜片,故B正确;
C.由发生电池反应为Zn+H2SO4═ZnSO4+H2↑,Cu不反应,铜为正极,Cu不易失电子而受到保护,故C正确;
D.原电池工作时,溶液中阳离子向正极Cu电极移动,且Cu极上发生的是还原反应,故D错误;
故答案为D。

【题目】某学生用邻苯二甲酸氢钾,(分子式为![]() 相对分子质量为204)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol/L左右,滴定终点时溶液的pH约为9.1。
相对分子质量为204)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol/L左右,滴定终点时溶液的pH约为9.1。
(1)写出邻苯二甲酸氢钾与NaOH反应的化学方程式:________。
(2)将用分析天平精确称量的邻苯二甲酸氢钾放于锥形瓶中,加适量的水溶解,溶液无色,再加入指示剂_____(从甲基橙、酚酞、石蕊中选择),用NaOH溶液滴定到终点时,现象是________。
(3)该实验要用到的主要玻璃仪器_______、______。
(4)该学生进行三次实验,所取固体的质量均相同,填写下表:
实验 编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
1 | 0.4488 | 22.24 |
2 | 20.04 | |
3 | 19.96 |
滴定中误差较大的是第_____次实验,造成这种误差的可能原因是_____
a.滴定时有NaOH溶液滴到锥形瓶外面;
b.未用NaOH溶液润洗滴定管;
c.NaOH溶液在“0”刻度线以上,未予调整就开始滴定;
d.观察记录滴定管内液面刻度时滴定前仰视,滴定后俯视;
e.酚酞指示剂由无色变为红色时立即停止滴定。
(5)NaOH溶液的物质的量浓度为______。