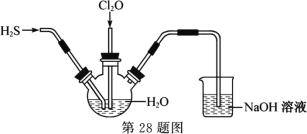
题目内容
【题目】A、X、Y、Z、Q、R、T 分别代表原子序数依次增大的短周期元素。元素A是原子半径最小的元素;X、Y、Z同周期且相邻,都是蛋白质的组成元素;X、R同族,Q与T原子的最外层电子数之和是R原子最外层电子数的2倍,T单质为淡黄色固体。U是d区元素,U2+的核外最高能级有2对成对电子。请回答下列问题:
(1)Y元素在周期表中的位置______,位于周期表______区;Q原子的核外电子排布式为______。
(2)X、Y、Z元素的第一电离能由大到小的顺序是______。
(3)TZ3分子为______分子(填“极性”或“非极性”),YZ2–离子实际构型是______。
(4)Z和T的简单气态氢化物稳定性好的是______(填化学式),原因是______。
(5)A、X、Z可形成分子式为A2XZ的有机物,则该化合物分子中X原子的轨道杂化类型是______;1mol该分子中含有π键的数目是______。(用“NA”表示)
【答案】第二周期第ⅤA族 p 1s22s22p63s2 N>O>C 非极性 V形 H2O 非金属性O>S,相应氢化物的稳定性:H2O>H2S sp2杂化 NA
【解析】
分析题给信息,元素A为原子半径最小的元素,则A为H元素;X、Y、Z原子序数依次增大、同周期且相邻,都是蛋白质的组成元素,则X为C元素,Y为N元素,Z为O元素。X、R同族,且都为短周期元素,则可知R为Si元素。T单质为淡黄色固体,可知T为S元素。由Q与T原子的最外层电子数之和是R原子最外层电子数的2倍,可知Q最外层电子数为2,且原子序数:O<Q<Si,则Q为Mg元素。U是d区元素,则U的最外层有1~2个电子,次外层有1~9个电子,根据U2+的核外最高能级有2对成对电子可知,U的价电子构型为3d74s2,U为Co元素,据此分析。
(1)Y为N元素,在元素周期表中位于第二周期第ⅤA族,位于元素周期表p区。Mg元素原子序数为12,其核外电子排布式为:1s22s22p63s2;答案为:第二周期第ⅤA族;p;1s22s22p63s2;
(2)根据同一周期元素的第一电离能总体上呈增大的趋势以及ⅤA族元素原子最外层为半充满状态,其第一电离能大于同周期相邻元素,可知C、N、O的第一电离能由大到小的顺序为:N>O>C;答案为:N>O>C;
(3)SO3分子的中心原子价层电子对数为![]() 且中心原子S上没有孤电子对,则SO3的分子立体构型为平面正三角形,SO3分子正负电荷重心重合,所以SO3为非极性分子。NO2-离子的中心原子价层电子对数为
且中心原子S上没有孤电子对,则SO3的分子立体构型为平面正三角形,SO3分子正负电荷重心重合,所以SO3为非极性分子。NO2-离子的中心原子价层电子对数为![]() ,且含1对孤电子对,则NO2-离子的实际构型为V形。答案为:非极性;V形;
,且含1对孤电子对,则NO2-离子的实际构型为V形。答案为:非极性;V形;
(4)Z和T的简单气态氢化物分别为H2O、H2S,因为非金属性O>S,根据非金属性越强,其相应氢化物的稳定性越强,可知稳定性好的是H2O。答案为:H2O;非金属性O>S,相应氢化物的稳定性:H2O>H2S;
(5)由分析可知,A2XZ的有机物为H2CO,该分子的中心原子价层电子对数为![]() ,中心原子无孤电子对,则H2CO的立体构型为平面三角形,所以H2CO中C原子的轨道杂化类型为sp2杂化,H2CO分子中存在C=O,C=O双键中有一个键为σ键,另一个键为π键,则1mol该分子中含有π键的数目是NA;答案为:sp2杂化;NA。
,中心原子无孤电子对,则H2CO的立体构型为平面三角形,所以H2CO中C原子的轨道杂化类型为sp2杂化,H2CO分子中存在C=O,C=O双键中有一个键为σ键,另一个键为π键,则1mol该分子中含有π键的数目是NA;答案为:sp2杂化;NA。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案【题目】研究发现,反应CCl4(g)+H2(g)![]() CHCl3(g)+HCl(g) ,可使CCl4(沸点77 ℃)转化为重要的化工原料CHCl3(沸点61.2 ℃),可减少其对臭氧层的破坏。(已知:该反应的副反应会生成CH2Cl2、CH3Cl和CH4等)
CHCl3(g)+HCl(g) ,可使CCl4(沸点77 ℃)转化为重要的化工原料CHCl3(沸点61.2 ℃),可减少其对臭氧层的破坏。(已知:该反应的副反应会生成CH2Cl2、CH3Cl和CH4等)
(1)CH4与Cl2反应时,每生成1molCCl4(g)或1molCHCl3(g)的焓变分别是△H1和△H2;H2在Cl2中燃烧,每生成1molHCl(g)产生的焓变为△H3,则:CCl4(g)+H2(g)![]() CHCl3(g)+HCl(g)的△H=_____(用含有△H1、△H2和△H3的算式表示)
CHCl3(g)+HCl(g)的△H=_____(用含有△H1、△H2和△H3的算式表示)
(2)在密闭容器中,CCl4+H2![]() CHCl3+HCl达到平衡状态后,测得如下数据(假设不考虑副反应)。
CHCl3+HCl达到平衡状态后,测得如下数据(假设不考虑副反应)。
实验序号 | 温度/℃ | 初始CCl4浓度/(mol·L-1) | 初始H2浓度/(mol·L-1) | CCl4的平衡转化率 |
1 | 110 | 0.8 | 1.2 | α1 |
2 | 110 | 1 | 1 | 50% |
3 | 100 | 1 | 1 | α3 |
①实验1中,CCl4的转化率α1_____50%(填“大于”“小于”或“等于”)。
②实验2中,反应进行到10h时达到平衡,在这10h内,H2的平均反应速率为_____mol· L-1·min-1。
③110 ℃时,该反应的化学平衡常数的数值为________。
④实验3中,α3的值________。
A. 等于50% B.大于50% C.小于50% D.依题所给信息无法判断
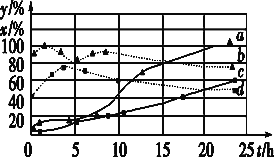
①图中表示H2起始浓度为2mol·L-1CHCl3的百分含量的变化曲线是____(填字母)。
②依图可知,有利于提高CCl4的消耗百分率和产物中CHCl3的百分含量H2的起始浓度应该为________mol·L-1。