题目内容
【题目】下列图示与对应的叙述相符合的是( )
A.图甲表示向CH3COOH溶液中逐渐加入少量CH3COONa固体后,溶液pH的变化
B.图乙表示用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1醋酸溶液的滴定曲线
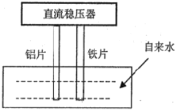
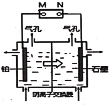
C.图丙表示电解法处理污水的原理,生成的胶体能除去污水中的悬浮物,该装置中的铁片可用铝片代替
D.图丁表示镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高
【答案】C
【解析】
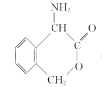
A.CH3COOH![]() CH3COO-+H+,加入少量CH3COONa固体,CH3COO-浓度增大,平衡逆向移动,H+浓度减小,pH增大,与图不符,A错误;
CH3COO-+H+,加入少量CH3COONa固体,CH3COO-浓度增大,平衡逆向移动,H+浓度减小,pH增大,与图不符,A错误;
B.醋酸是弱电解质,0.1000mol·L-1醋酸溶液,氢离子浓度小于0.1000mol·L-1,pH大于1,与图不符,B错误;
C. 实质是阳极Fe失电子生成Fe2+,阴极2H2O+2e-=H2↑+2OH-,Fe2+和OH-结合成Fe(OH)2,Fe(OH)2被氧化成Fe(OH)3胶体,Fe(OH)3胶体吸附污水中的悬浮物,换成Al后,阳极Al失电子生成Al3+,最终产生Al(OH)3胶体同样可以吸附污水中的悬浮物,C正确;
D. 从图丁曲线变化趋势可知,O→t1,反应放热,温度升高对化学反应速率的影响大于H+浓度降低对化学反应速率的影响,曲线呈上升趋势,但不能说明在t1时溶液的温度最高,D错误。
答案选C。

【题目】已知25℃时有关弱电解质的电离平衡常数:
弱电解质化学式 | CH3COOH | NH3·H2O | H2CO3 |
电离平衡常数(25℃) | 1.8×10-5 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 |
在25℃时,下列有关电解质溶液的说法不正确的是
A.pH相等的四种溶液a. CH3COONa b.Na2CO3 c. NaHCO3 d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d<b<c<a
B.0.1mol·L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.1L 0.50mol·L-1NH4Cl溶液与2L0.25mo·L-1NH4Cl溶液,前者含NH4+物质的量多
D.浓度均为0.1mol·L-1的CH3COOH、CH3 COONa混合溶液中: c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+)