题目内容
在一个容积为2L的密闭容器中,充入1mol SO2和1mol O2,一定条件下发生反应2SO2+O2?2SO3,2分钟后测得SO2的物质的量为0.6mol,则用SO2和O2表示的化学反应速率分别是 mol/(L?min)、 mol/(L?min),二者的关系是 .
考点:化学反应速率和化学计量数的关系
专题:化学反应速率专题
分析:根据v=
计算v(SO2)、v(O2),进而计算速率之比可以得出化学反应速率之比等于其化学计量数之比.
| △c |
| △t |
解答:
解:2分钟内SO2消耗1mol-0.6mol=0.4 mol,根据方程式,则O2消耗0.2 mol,
v(SO2)=
=
=0.1 mol/(L?min),
v(O2)=
=
=0.05 mol/(L?min)
v(SO2):v(O2)=0.1mol/(L?min):0.05 mol/(L?min)=2:1,即速率之比等于其化学计量数之比.
故答案为:0.1;0.05;SO2和O2的化学反应速率之比等于其化学计量数之比.
v(SO2)=
| △c |
| △t |
| 0.4mol/2L |
| 2min |
v(O2)=
| △c |
| △t |
| 0.2mol/2L |
| 2min |
v(SO2):v(O2)=0.1mol/(L?min):0.05 mol/(L?min)=2:1,即速率之比等于其化学计量数之比.
故答案为:0.1;0.05;SO2和O2的化学反应速率之比等于其化学计量数之比.
点评:本题考查化学反应速率有关计算,比较基础,注意对公式的理解与灵活应用及对速率规律的理解.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
在某温度下,可逆反应mA(g)+nB(g)?pC(g)+qD(g)的平衡常数为K,下列说法正确的是( )
| A、平衡常数发生变化,化学平衡必发生移动 |
| B、化学平衡发生移动,平衡常数必发生变化 |
| C、反应物的转化率越大,达到平衡时,K值越大 |
| D、温度越高,达到平衡时,K值越大 |
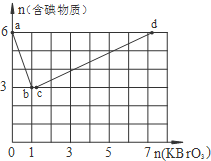 在稀硫酸酸化的含6mol KI溶液中逐滴加入KBrO3溶液,整个过程中含碘物质与所加入KBrO3物质的量的关系如图.请回答下列问题:
在稀硫酸酸化的含6mol KI溶液中逐滴加入KBrO3溶液,整个过程中含碘物质与所加入KBrO3物质的量的关系如图.请回答下列问题: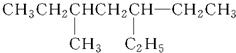 :
: :
: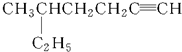
 :
: