题目内容
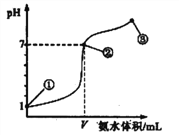
【题目】室温下某水溶液中的![]() 、
、![]() 浓度变化曲线如图所示,下列说法不正确的是
浓度变化曲线如图所示,下列说法不正确的是

A.向蒸馏水中加入NaOH固体充分溶解后恢复至室温,溶液最终可能落在b点
B.![]() 与HCl的混合溶液中水电离出的
与HCl的混合溶液中水电离出的![]() 浓度可能等于d点坐标
浓度可能等于d点坐标
C.若b点表示盐NaR的水溶液,向其中逐滴滴入过量的HR溶液,会引起b向c的变化
D.若c点表示某温度下盐NaHA的水溶液,则![]()
【答案】C
【解析】
A.向蒸馏水中加入NaOH固体,![]() 增大,水的电离平衡左移,
增大,水的电离平衡左移,![]() 减小,充分溶解后恢复至室温,溶液最终可能落在b点,故A正确;
减小,充分溶解后恢复至室温,溶液最终可能落在b点,故A正确;
B.![]() 水解促进水的电离,水电离出的
水解促进水的电离,水电离出的![]() 浓度可能等于d点纵坐标,故B正确;
浓度可能等于d点纵坐标,故B正确;
C.若b点表示盐NaR的水溶液,则![]() 水解溶液呈碱性,向其中逐滴滴入过量HR溶液,水解平衡逆向移动,
水解溶液呈碱性,向其中逐滴滴入过量HR溶液,水解平衡逆向移动,![]() 减小,b、c点
减小,b、c点![]() 相同,不会引起b向c的变化,故C错误;
相同,不会引起b向c的变化,故C错误;
D.若c点表示某温度下盐NaHA的水溶液,溶液呈碱性![]() ,
,![]() 的水解大于电离,
的水解大于电离,![]() ,则
,则![]() ,故D正确;
,故D正确;
故选C。

练习册系列答案
相关题目
【题目】在一定温度下,10mL0.40mol/L H2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)![]()
![]() mol/(L·min)
mol/(L·min)
B.6~10min的平均反应速率:v(H2O2)<![]() mol/(L·min)
mol/(L·min)
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%