题目内容
K3[Fe(C2O4)3]·3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂。实验室可用铁屑为原料制备,相关反应的化学方程式为:Fe+H2SO4 FeSO4+H2↑
FeSO4+H2↑
FeSO4+H2C2O4+2H2O FeC2O4·2H2O↓+H2SO4
FeC2O4·2H2O↓+H2SO4
2FeC2O4·2H2O+H2O2+H2C2O4+3K2C2O4 2K3[Fe(C2O4)3]+6H2O
2K3[Fe(C2O4)3]+6H2O
2Mn +5C2
+5C2 +16H+
+16H+ 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
回答下列问题:
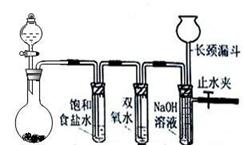
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收。下列吸收装置正确的是 。 
(2)在将Fe2+氧化的过程中,需控制溶液温度不高于40 ℃,理由是 ;得到K3[Fe(C2O4)3]溶液后,加入乙醇的理由是 。
(3)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤ (叙述此步操作),⑥计算。步骤③若未在干燥器中进行,测得的晶体中所含结晶水含量 (填“偏高”“偏低”或“无影响”);步骤⑤的目的是 。
(4)晶体中C2 含量的测定可用酸性KMnO4标准溶液滴定。称取三草酸合铁(Ⅲ)酸钾晶体m g溶于水配成250 mL溶液,取出20.00 mL放入锥形瓶中,用0.010 0 mol·L-1酸化的高锰酸钾溶液进行滴定。
含量的测定可用酸性KMnO4标准溶液滴定。称取三草酸合铁(Ⅲ)酸钾晶体m g溶于水配成250 mL溶液,取出20.00 mL放入锥形瓶中,用0.010 0 mol·L-1酸化的高锰酸钾溶液进行滴定。
①下列操作及说法正确的是 。
A.滴定管用蒸馏水洗涤后,即可装入标准溶液
B.装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量标准液,使尖嘴充满液体
C.接近终点时,需用蒸馏水冲洗瓶壁和滴定管尖端悬挂的液滴
②有同学认为该滴定过程不需要指示剂,那么滴定终点的现象为 ,若达到滴定终点消耗高锰酸钾溶液V mL,那么晶体中所含C2 的质量分数为 (用含V、m的式子表示)。
的质量分数为 (用含V、m的式子表示)。
(1)A (2)防止H2O2分解 三草酸合铁(Ⅲ)酸钾在乙醇中溶解度小 (3)重复②~④步操作至恒重 偏低 检验晶体中的结晶水是否已全部失去
(4)①B ②当滴入最后一滴KMnO4溶液,锥形瓶中溶液恰好由无色变为浅红色,且半分钟不褪色 
解析

某研究性学习小组为测定NH3分子中氮、氢原子个数比,设计如下实验流程:
实验时,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。
下图A、B、C为该小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。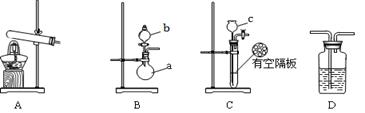
请回答下列问题:
(1)写出仪器的名称:a ,b 。
(2)硬质玻璃管中发生的反应方程式是 ,反应过程中硬质玻璃管的现象是 。
(3)请判断制取氨气可能用到的装置,在下表中你认为可行的装置中填写对应的实验药品(写出化学式)。
| 装置 | 实验药品 |
| A | |
| B | b: a: |
| C | c: 隔板: |
(4)实验时洗气瓶D中的浓硫酸表现 性;该小组实验测得:洗气前装置D的质量为m1g、洗气后装置D的质量为m2g、生成的氮气在标准状况下的体积为V L。根据该小组计算NH3分子中氮、氢的原子个数比的表达式,请预计该结果与理论值相比, 。
A.在实验误差范围内数值接近理论值 B.数值偏高 C.数值偏低
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源。
(1)某兴趣小组采用如图所示装置制取SO2
①下列实验方案适用如图所示装置制取所需SO2的试剂是_______(填序号)。
| A.Na2SO3溶液与稀硝酸 |
| B.Na2SO3固体与浓硫酸 |
| C.固体硫和氧气 |
| D.铜与浓硫酸 |
③尾气吸收装置的连接顺序是b接( )接 ( )接e。
(2)为了回收利用SO2废气,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体(
 生产流程,其流程示意图如下:
生产流程,其流程示意图如下:
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时溶液的pH见下表:

请回答:
①含Al3+的盐常用作净水剂,用离子方程式表示其净水原理________________________。
②浸出过程中主要反应的化学方程式是___________________________________________。
③氧化过程中加入MnO2粉的目的是______________________________________________;
反应的离子方程式是_________________________________________________________。
④用石灰浆调节pH,pH应调节的范围是___________________________________。
⑤滤渣的主要成分是____________________________________。
用下列实验装置进行的实验中,不能达到相应实验目的的是 ( )
| A.装置甲:气体从b口进入,收集CO2 | B.装置乙:可制得金属锰 |
| C.装置丙:实验室制取乙酸乙酯 | D.装置丁:验证HCl气体在水中的溶解性 |