题目内容
17.3×6.02×1023个电子的物质的量是3mole-.分析 根据n=$\frac{N}{{N}_{A}}$计算电子物质的量.
解答 解:根据n=$\frac{N}{{N}_{A}}$得电子物质的量=$\frac{3×6.02×1{0}^{23}}{6.02×1{0}^{23}/mol}$=3mol,故答案为:3.
点评 本题考查物质的量有关计算,侧重考查学生计算能力,明确n、N、NA之间关系即可解答,题目难度不大.

练习册系列答案
相关题目
7.下列反应属氧化还原的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | H2+Cl2═HCl | C. | Na2O+H2O═2NaOH | D. | NH3+HCl═NH4Cl |
5.在通风橱中进行下列实验:
下列说法中不正确的是( )
| 步骤 | 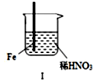 |  | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe Cu接触后,其表面均产生红棕色气泡 |
| A. | Ⅰ中气体有无色变红棕色的化学方程式为:2NO+O2=2NO2 | |
| B. | 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| C. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
2.实验室中可用KClO3和浓HCl反应制取氯气,写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目 ;该反应中,氧化产物是Cl2,还原产物是Cl2,氧化产物与还原产物的物质的量之比是5:1.
;该反应中,氧化产物是Cl2,还原产物是Cl2,氧化产物与还原产物的物质的量之比是5:1.
 ;该反应中,氧化产物是Cl2,还原产物是Cl2,氧化产物与还原产物的物质的量之比是5:1.
;该反应中,氧化产物是Cl2,还原产物是Cl2,氧化产物与还原产物的物质的量之比是5:1.
9.HCl+NaOH═NaCl+H2O的反应类型是( )
| A. | 化合反应 | B. | 置换反应 | C. | 分解反应 | D. | 复分解反应 |
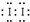 (用电子式表示).
(用电子式表示).