题目内容
一定浓度l00mL的HNO3溶液中加入2.8gFe,全部溶解,得到标准状况下的NO气体1.12L, 测得反应后溶液中的c(H+)=0.1mol/L。若反应前后溶液体积变化忽略不计,则下列有关判断错误的是
| A.反应后溶液中无硝酸亚铁 |
B.反应前HNO3溶液的浓度为2.0mol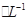 |
C.反应后溶液中c(NO3-)=1.6mol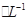 |
| D.反应后的溶液最多还能溶解1.6lgFe |
B
解析试题分析:由信息知道反应后硝酸剩余,所以反应后溶液中无硝酸亚铁,A正确;反应前硝酸的物质的量="3×2.8/56+1.12/22.4+0.01=0.15+0.05+0.01=0.21mol." 反应前HNO3溶液的浓度为2.1mol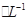 ,所以B错误;反应后溶液中n(NO3-)=" 3×2.8/56+0.01=0.16mol," c(NO3-)=1.6mol
,所以B错误;反应后溶液中n(NO3-)=" 3×2.8/56+0.01=0.16mol," c(NO3-)=1.6mol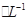 ,C正确;原硝酸能溶解的Fe的最大质量为 0.21mol×3/8×56= 4.41g,故 能再溶解的Fe的质量为4.41g-2.8g=1.61g故D正确( 3 Fe+8HNO3=3Fe(NO3)2 +2 NO↑+4H2O (稀硝酸不足)。
,C正确;原硝酸能溶解的Fe的最大质量为 0.21mol×3/8×56= 4.41g,故 能再溶解的Fe的质量为4.41g-2.8g=1.61g故D正确( 3 Fe+8HNO3=3Fe(NO3)2 +2 NO↑+4H2O (稀硝酸不足)。
考点:金属和硝酸的反应,计算。

在下列各氧化还原反应中,水既不作氧化剂,也不作还原剂的是
| A.2F2+2H2O=4HF+O2↑ | B.C+H2O CO+H2 CO+H2 |
| C.2Na+2H2O=2NaOH+H2↑ | D.3NO2+H2O=2HNO3+NO |
将一定量氯气通入溴化亚铁溶液后,再加入四氯化碳,振荡,静置,整个过程中肯定能观察到的现象
| A.水层显棕黄色 | B.水层无色 | C.四氯化碳层显红棕色 | D.四氯化碳层无色 |
制备Fe3O4纳米颗粒的总反应如下:3Fe2++ 2S2O32-+O2+4OH-= Fe3O4 + S4O62-+2H2O。下列说法正确的是
| A.当转移1mol电子时,消耗56g S2O32- |
| B.在反应中硫元素被氧化,铁元素被还原 |
| C.还原剂是Fe2+,氧化剂是S2O32-和O2 |
| D.每生成1mol Fe3O4,转移3mol电子 |
将6.85g Fe和Al的混合物溶于200mL 浓度为C mol/L的HNO3溶液中,得到标准状况下的NO、N2O混合气体共3.36L,测得反应后溶液的pH为0,再向所得溶液中加入过量NaOH溶液充分反应后生成沉淀质量为5.35 g。若不考虑反应前后溶液体积变化,则下列有关判断正确的是( )。
| A.Fe与Al 的物质的量之比为1:1 |
| B.混合气体中NO为0.03mol ,N2O为0.12mol |
| C.原HNO3溶液的浓度C=4.9mol/L |
| D.反应中被还原的HNO3为0.15mol |
往AgNO3、Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后,发现有少量金属析出,过滤后往滤液中滴加盐酸有白色沉淀生成,则析出的少量金属一定是
| A.Ag | B.Cu | C.Fe | D.Zn |
氧化还原反应与四种基本反应类型的关系如图所示。下列化学反应属于阴影部分的是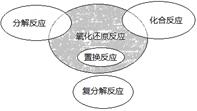
| A.4NH3 +5O2 =4NO+6 H2O |
| B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.2NaHCO3=Na2CO3+H2O+CO2↑ |
| D.Cl2+2NaBr=2NaCl +Br2 |
根据表中信息判断,下列选项不正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4 、H2O2 、H2SO4 | K2SO4 、MnSO4 ...... |
| ② | Cl2 、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- ...... | Cl2 、Mn2+ ...... |
A.第①组反应的其余产物为H2O和 O2
B.第②组反应中Cl2 与 FeBr2的物质的量之比小于或等于1︰2
C.第③组反应中生成1mol Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4- > Cl2 > Fe3+ > Br2
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2.24 L NO,剩余9.6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下2.24 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法中正确的是( )
| A.原混合物中铜和铁各0.15 mol |
| B.稀硝酸的物质的量浓度为1 mol·L-1 |
| C.第一次剩余9.6 g金属为铜和铁 |
| D.再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO |