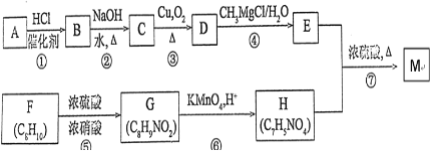
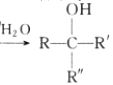
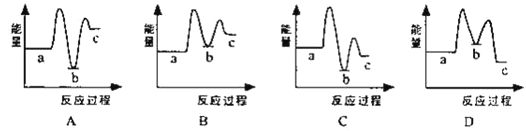
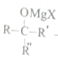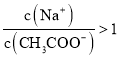题目内容
【题目】![]() 定温度下,下列溶液的离子浓度关系式正确的是
定温度下,下列溶液的离子浓度关系式正确的是![]()
A.![]() 的
的![]() 溶液中,
溶液中,![]()
B.稀释氨水溶液10倍后,其![]() 为原來的
为原來的![]()
C.pH之和为14的![]() 与NaOH溶液混合:
与NaOH溶液混合:![]()
D.将等物质的量的![]() 和
和![]() 混合溶于水中:
混合溶于水中:
【答案】D
【解析】
A.根据硫化氢溶液中的电离平衡![]() 、
、![]() 、
、![]() 判断;
判断;
B.一水合氨为弱碱,弱碱在稀释过程中溶液中的氢氧根离子浓度变化比强碱溶液小;
C.pH之和为14的![]() 与NaOH溶液混合溶液中存在电荷守恒;
与NaOH溶液混合溶液中存在电荷守恒;
D.将等物质的量的![]() 和
和![]() 混合溶于水中,碳酸根离子水解程度大于碳酸氢根离子。
混合溶于水中,碳酸根离子水解程度大于碳酸氢根离子。
![]() 溶液中存在电离平衡:
溶液中存在电离平衡:![]() 、
、![]() 、
、![]() ,根据上述反应知,氢离子来自水的电离和硫化氢的电离,则
,根据上述反应知,氢离子来自水的电离和硫化氢的电离,则![]() 的
的![]() 溶液中,
溶液中,![]()
![]() ,故A错误;
,故A错误;
B.一水合氨为弱电解质,加水稀释后促进了其电离,溶液中的氢氧根离子浓度变化比强碱溶液小,其![]() 比原來的
比原來的![]() 大,故B错误;
大,故B错误;
C.pH之和为14的![]() 与NaOH溶液混合,溶液中电荷守恒为:
与NaOH溶液混合,溶液中电荷守恒为:![]() ,故C错误;
,故C错误;
D.碳酸根离子水解程度大于碳酸氢根离子,将等物质的量的![]() 和
和![]() 混合溶于水中
混合溶于水中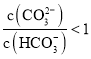 ,故D正确;
,故D正确;
故选:D。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目