��Ŀ����
����Ŀ����������M��һ��ҩ�����Ҫ�ϳ��м��壬��ϳ�·�����£�

��֪������Ϣ��
�ٷ�����A����Է���������100��110֮�䣬1molA��ȫȼ�տ�����10molO2��
��H�ĺ˴Ź���������ʾ����3���⡣
��RCH=CH2![]() RCHClCH3
RCHClCH3
��RX+Mg![]() RMgX(X����±��)
RMgX(X����±��)
��
![]()


�ش��������⣺
(1)A�Ľṹ��ʽΪ______��H�й����ŵ�����Ϊ______��
(2)��E��H����M�Ļ�ѧ����ʽΪ______��
(3)����������Ӧ����______(�����)��
(4)ͬʱ��������������E��ͬ���칹����______��(�����������칹)�����б�����һ�ȴ���ֻ�����ֵĽṹ��ʽΪ______��(��дһ��)
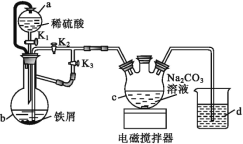
������̼������Һ������Ӧ���ڱ����ϵ�ȡ������Ŀ��2��
(5)����������Ϣ���ɱ��ϳɱ���ϩ���ϳ�·����ͼ��ʾ����ش��������⡣

�Լ���Ϊ______�����һ����Ӧ�Ļ�ѧ����ʽΪ______��
���𰸡�![]() �Ȼ�������
�Ȼ������� 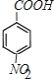 +
+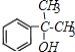
![]()
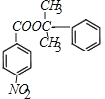 +H2O
+H2O ![]() 6
6 ![]() ��
��![]() �� CH3CHO
�� CH3CHO ![]()
![]()
![]() +H2O
+H2O
��������
������A����Է���������100��110֮�䣬1molA��ȫȼ�տ�����10molO2����A�ķ���ʽΪCxHy����x+![]() =10����ϸ������ķ���ʽͨʽ��ͨ�����ۣ��ɵõ������ʷ���ʽΪC8H8��A�ܹ���HCl�����ӳɷ�Ӧ����B����A�Ľṹ��ʽΪ
=10����ϸ������ķ���ʽͨʽ��ͨ�����ۣ��ɵõ������ʷ���ʽΪC8H8��A�ܹ���HCl�����ӳɷ�Ӧ����B����A�Ľṹ��ʽΪ![]() ��������Ϣ�ۿ�֪B�Ľṹ��ʽΪ
��������Ϣ�ۿ�֪B�Ľṹ��ʽΪ![]() ��B���������Ƶ�ˮ��Һ�м�������C����CΪ
��B���������Ƶ�ˮ��Һ�м�������C����CΪ![]() ��C����������D����DΪ
��C����������D����DΪ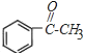 �������Ϣ�ݿ�֪EΪ
�������Ϣ�ݿ�֪EΪ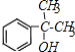 ��F����������Ӧ����G��G�����Ը��������Һ��������H��H�ĺ˴Ź������ױ�����3�ֲ�ͬ��ѧ�������⣬��HΪ
��F����������Ӧ����G��G�����Ը��������Һ��������H��H�ĺ˴Ź������ױ�����3�ֲ�ͬ��ѧ�������⣬��HΪ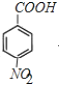 ��GΪ
��GΪ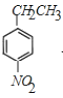 ��H��E����������Ӧ����M����MΪ
��H��E����������Ӧ����M����MΪ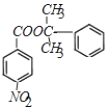 ���Դ˽����⡣
���Դ˽����⡣
(1)���ݷ�����֪��A�Ľṹ��ʽΪ��![]() ��HΪ
��HΪ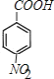
(2)EΪ ��HΪ
��HΪ �����߷���������Ӧ�γ���M�Ļ�ѧ����ʽΪ��
�����߷���������Ӧ�γ���M�Ļ�ѧ����ʽΪ�� +
+
![]()
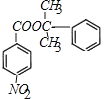 +H2O��
+H2O��
(3)�������̿�֪����Ӧ��Ϊ�ӳɷ�Ӧ����Ӧ��Ϊȡ����Ӧ����Ӧ��Ϊ������Ӧ����Ӧ��Ϊ�ӳɷ�Ӧ����Ӧ��Ϊȡ����Ӧ����Ӧ��Ϊ������Ӧ����Ӧ��Ϊ������Ӧ��Ҳ����ȡ����Ӧ����Ӧ��������������Ӧ��Ϊ�ۢޣ�
(4)E�Ľṹ��ʽΪ ��E��ͬ���칹���������������������̼������Һ������Ӧ��˵�����л�������к��з��ǻ����ڱ�����������ȡ�������������������л�������б��������ӵ�������������Ϊ��-OH��-CH2CH2CH3��-OH��-CH(CH3)2������2�������ÿ�ֺ����ڡ��䡢������ͬ���칹�壬�������������Ľṹ��ʽ����Ϊ��2��3=6�֣����б�����һ�ȴ���ֻ�����֣�˵������жԳƽṹ�����������Ľṹ��ʽΪ��
��E��ͬ���칹���������������������̼������Һ������Ӧ��˵�����л�������к��з��ǻ����ڱ�����������ȡ�������������������л�������б��������ӵ�������������Ϊ��-OH��-CH2CH2CH3��-OH��-CH(CH3)2������2�������ÿ�ֺ����ڡ��䡢������ͬ���칹�壬�������������Ľṹ��ʽ����Ϊ��2��3=6�֣����б�����һ�ȴ���ֻ�����֣�˵������жԳƽṹ�����������Ľṹ��ʽΪ��![]() ��
��![]() ��
��
(5)�������Ϣ��֪�Լ���ΪCH3CHO�����һ��������ȥ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ![]()
![]()
![]() +H2O��
+H2O��

����Ŀ����.��Դ�ǹ��÷�չ����Ҫ�������ҹ�Ŀǰʹ�õ���Դ��Ҫ�ǻ�ʯȼ�ϡ�
��֪��C��s����O2��g��===CO2��g������H1����393.5 kJ��mol��1
H2��g����![]() O2��g��===H2O��g������H2����241.8 kJ��mol��1
O2��g��===H2O��g������H2����241.8 kJ��mol��1
CO��g����![]() O2��g��===CO2��g������H3����283.0 kJ��mol��1
O2��g��===CO2��g������H3����283.0 kJ��mol��1
��ú������Ҫ��ӦC��s����H2O��g��=CO��g����H2��g������H��____________________��
��.Ϊ�˼���CO���ŷţ�ij�����о�С����CO��H2Ϊԭ�Ϻϳ������Դ�����ѣ�DME������Ӧ���£�4H2��g����2CO��g��![]() CH3OCH3��g����H2O��g������H����198 kJ��mol��1��
CH3OCH3��g����H2O��g������H����198 kJ��mol��1��
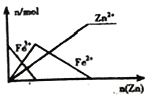
��1����ͼ��ʾ����ȷ��ӳƽ�ⳣ��K���¶ȱ仯��ϵ������Ϊ________�������߱����ĸ�������ж�������____________��

��2����һ���¶��£���2.0 L�̶��ݻ����ܱ������г���2 mol H2��1 mol CO������һ��ʱ���Ӧ4H2��g����2CO��g��![]() CH3OCH3��g����H2O��g���ﵽƽ�⡣��Ӧ�����в�õIJ������ݼ��±���
CH3OCH3��g����H2O��g���ﵽƽ�⡣��Ӧ�����в�õIJ������ݼ��±���
ʱ��/min | 0 | 20 | 40 | 80 | 100 |
n��H2��/mol | 2.0 | 1.4 | 0.85 | 0.4 | �� |
n��CO��/mol | 1.0 | �� | 0.425 | 0.2 | 0.2 |
n��CH3OCH3��/mol | 0 | 0.15 | �� | �� | 0.4 |
n��H2O��/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
��0��20 min��ƽ����Ӧ����v��CO����__________________mol��L��1��min��1��
�ڴﵽƽ��ʱ��H2��ת����Ϊ__________________��
���������¶��£��÷�Ӧ��ƽ�ⳣ��K��______________________��
���ܱ����÷�Ӧ�ﵽƽ��״̬����________������ţ���
A CO��ת���ʵ���H2O�IJ��� B ��������ƽ����Է�����������
C v��CO����v��H2���ı�ֵ���� D ���������ܶȲ���
���������¶��£���ƽ����2 L�������ٳ���0.4 mol H2��0.4 mol CH3OCH3��g������ѧƽ��________�ƶ���������������������������������