题目内容
【题目】下列离子方程式书写正确的是( )
A.Ba(OH)2和H2SO4两溶液混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.氯气溶于水:H2O+Cl2= 2H++ Cl-+ClO-
C.锌和硝酸银溶液反应:Zn+Ag+=Ag+Zn2+
D.向Al2(SO4)3溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
【答案】D
【解析】
A.![]() 是二元强碱,
是二元强碱,![]() 是二元强酸,两者反应的离子方程式是
是二元强酸,两者反应的离子方程式是![]() ,A项错误;
,A项错误;
B.次氯酸是弱酸,不能拆开,离子方程式为Cl2+H2O=H++Cl-+HClO,B项错误;
C.选项中电荷不守恒,正确的离子方程式是![]() ,C项错误;
,C项错误;
D.氨水是弱碱水溶液,过量的氨水只能与![]() 反应得到
反应得到![]() ,D项正确;
,D项正确;
答案选D。

练习册系列答案
相关题目
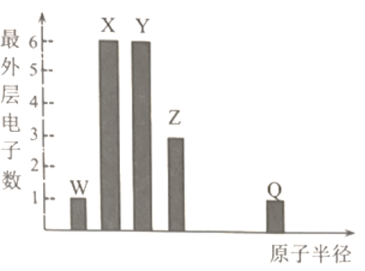
【题目】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是5种元素的相关信息,W、X都位于第三周期。
元素 | 信息 |
Q | 地壳中含量最高的元素 |
W | 最高化合价为+7价 |
X | 最高价氧化物对应的水化物在本周期中碱性最强 |
Y | 焰色试验(透过蓝色钴玻璃)火焰呈紫色 |
Z | 原子结构示意图为: |
(1)Q在周期表中的位置是__。
(2)W的最高价氧化物对应的水化物的化学式是___。
(3)X单质与水反应的离子方程式是__。
(4)金属性Y强于X,用原子结构解释原因:__,失电子能力Y大于X,金属性Y强于X。
(5)下列对于Z及其化合物的推断中,正确的是__(填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质可与X和W形成的化合物的水溶液发生置换反应