题目内容
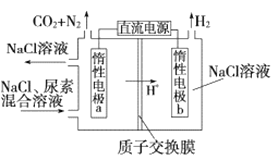
【题目】甲醇燃料电池能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注,其工作示意图如图,其总反应为:2CH3OH+3O2=2CO2+4H2O。下列说法不正确的是

A. 电极A是负极,发生氧化反应
B. 电池工作时,电解液中的H+通过质子交换膜向B电极迁移
C. 放电前后电解质溶液的pH不变
D. b物质在电极上发生的电极反应式为:O2+4e-+4H+=2H2O
【答案】C
【解析】
A.根据图示,电子由A极流出,沿导线流向B极,则A为负极、B为正极,A极发生氧化反应,故A正确;
B.原电池工作时,电解质溶液中阳离子H+向正极B移动,故B正确;
C.电池反应式为2CH3OH+3O2═2CO2+4H2O,有水生成导致溶液体积增大,溶质浓度减小,则c(H+)减小,所以溶液的pH增大,故C错误;
D.正极上氧气得电子和氢离子反应生成水,正极的电极反应式为:O2+4e-+4H+=2H2O,故D正确;
故选C。

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目