题目内容
【题目】X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示![]() 水及部分产物已略去
水及部分产物已略去![]() .
.
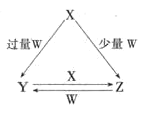
(1)若X为金属单质,W是某强酸的稀溶液.X与过量W反应生成Y的离子方程式为 ______ ;组成X的元素在周期表中的位置是 ______ .
(2)若X为非金属单质,W是空气的主要成分之一.它们之间转化的能量变化如图A所示,则X+W→Z的热化学方程式为 ______ .
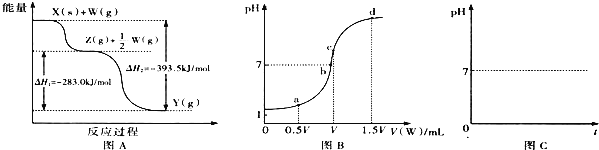
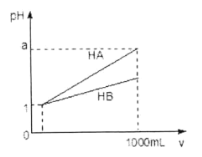
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),则X与过量W反应生成Y的离子方程式为 ______ ![]() 室温下,若用0.1mol/L的W溶液滴定VmL0.1mol/LHA溶液,滴定曲线如图B所示,则a、b、c、d四点溶液中水的电离程度最大的是 ______ 点;a点溶液中离子浓度的大小顺序为 ______ .
室温下,若用0.1mol/L的W溶液滴定VmL0.1mol/LHA溶液,滴定曲线如图B所示,则a、b、c、d四点溶液中水的电离程度最大的是 ______ 点;a点溶液中离子浓度的大小顺序为 ______ .
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物.常温时,将Z的水溶液露置于空气中,请在图C中画出其pH随时间(t)的变化趋势曲线图![]() 不考虑水的挥发
不考虑水的挥发![]() ______ .
______ .
【答案】Fe+4H++NO3-= Fe3++NO↑+2H2O 第四周期VIII族 C(s)+![]() O2(g)=CO(g) H=-110.5kJ/mol Al3++4OH-=AlO2-+2H2O c c(A-)>c(M+) >c(H+)>c(OH-)
O2(g)=CO(g) H=-110.5kJ/mol Al3++4OH-=AlO2-+2H2O c c(A-)>c(M+) >c(H+)>c(OH-) 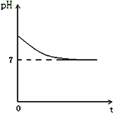
【解析】
(1)若X为金属单质,W是某强酸的稀溶液,由转化关系可知,X为变价金属为Fe,W为硝酸,Y是硝酸铁,Z是硝酸亚铁;
(2)若X为非金属单质,X和W反应生成物与W的量有关,则X是变价元素,W是空气的主要成分之一,则X为碳、W为氧气,Y是二氧化碳,Z是一氧化碳;
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),X为铝盐、Y为偏铝酸盐、Z为氢氧化铝;
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物,则W为SO2、Z为亚硫酸盐,Y为亚硫酸氢盐。
(1)若X为金属单质,W是某强酸的稀溶液,由转化关系可知,X为变价金属为Fe,W为硝酸,Y是硝酸铁,Z是硝酸亚铁,铁和过量硝酸反应生成硝酸铁、一氧化氮和水,离子方程式为:Fe+4H++NO3-= Fe3++NO↑+2H2O,铁位于第四周期VIII族,
(2)若X为非金属单质,X和W反应生成物与W的量有关,则X是变价元素,W是空气的主要成分之一,则X为碳、W为氧气,Y是二氧化碳,Z是一氧化碳,碳和少量氧气反应生成一氧化碳,根据图知H=-393.5-(-283.0)=-110.5kJ/mol,所以该热化学反应方程式为C(s)+![]() O2(g)=CO(g) H=-110.5kJ/mol;
O2(g)=CO(g) H=-110.5kJ/mol;
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),X为铝盐、Y为偏铝酸盐、Z为氢氧化铝,铝离子和过量强碱反应生成偏铝酸盐和水,离子方程式为Al3++4OH-=AlO2-+2H2O,酸或碱抑制水电离,含有弱根离子的盐促进水电离,根据图知,a、b点酸过量,d碱过量,c点二者恰好反应生成强碱弱酸盐,则水的电离程度最大,a点溶液中溶质是等物质的量浓度的HA和MA,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒得c(H+)+ c(M+)=c(OH-)+ c(A-),所以c(A-)>c(M+),酸的电离程度较小,所以c(M+)> c(H+),则离子浓度大小顺序是c(A-)>c(M+) >c(H+)>c(OH-);
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物,则W为SO2、Z为亚硫酸盐,Y为亚硫酸氢盐,Z是亚硫酸盐,为强酸弱碱盐,亚硫酸根离子水解生成亚硫酸,亚硫酸不稳定,易被氧气氧化生成硫酸,硫酸是强电解质,完全电离导致溶液中氢离子浓度增大,溶液的酸性增强,则pH逐渐减小,所以其图象为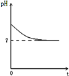 。
。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】用浓盐酸和二氧化锰制氯气的实验装置如图所示:

(1)下列气体实验室制备时,可以用相同发生装置的是 _______
A.O2 B. H2 C.HCl D. CO2
(2)制得的氯气中还含有氯化氢杂质,可通过装有______的洗气瓶除去。
(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为___________;漂白粉在空气中很容易变质,请写出漂白粉在空气中变质的反应方程式____。
(4)据报道,日常生活中,将洁厕液(主要成分是HCl)与84消毒液(主要成分是次氯酸钠)混合使用会发生中毒的事故,生成有毒的氯气。写出反应的化学方程式______。
(5)二氧化锰和高锰酸钾都是强氧化剂,均可将浓盐酸氧化为氯气。用浓盐酸和高锰酸钾制氯气的反应方程式如下: KMnO4 + HCl= KCl + MnCl2 + Cl2↑+ H2O
①配平该反应的化学方程式______。
②用“单线桥”在上述方程式上标出电子转移的方向和数目______。该反应中______元素被氧化,起酸性作用的HCl是______mol。当有1mol电子转移时,可生成气体(标准状态下)______ 升。
(6)(如图)有人做了一个改进实验。挤压软塑料瓶,向装有固体B的锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可以看到明显的燃烧现象(金属网用以防止气体混合爆炸)。

①用此装置模拟工业合成盐酸。则相应试剂选择正确的是_________(选填序号)。
溶液A | 固体B | 气体C | |
a | 稀硫酸 | Zn | Cl2 |
b | 浓盐酸 | MnO2 | H2 |
c | 稀硝酸 | Fe | Cl2 |
d | 浓盐酸 | KMnO4 | H2 |
②管口可观察到的现象是__________。