��Ŀ����
����Ŀ���о�����ȿ���CO��CO2��Ӧ�þ�����Ҫ���������.�ش��������⣺
I.CO�����ڸ�¯��������֪��
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2 (g) ��H1=akJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2 (g) �� H2=bkJ/mol
��ӦFe2O3(s)+3CO(g)=2Fe(s)++3CO2 (g)����H=______kJ/mol
��.���������£�CO2��CO���Ի���ת��
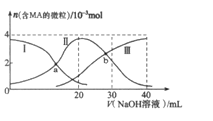
(1)ij�¶��£����ݻ�Ϊ2 L���ܱ��������ס������ַ�ʽͶ�뷴Ӧ�����Ӧ��
CO2 (g)+H2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)

������15 min��ﵽƽ�⣬��ʱCO2��ת����Ϊ75%����015 min��ƽ����Ӧ����_______���������¸÷�Ӧ��ƽ�ⳣ��K= ____����ʹƽ������������ͬ�����������������ȣ���w��x��y��z������Ĺ�ϵ��: y____z(����������������� = ��)����y=_________(�ú��ĵ�ʽ��ʾ)��
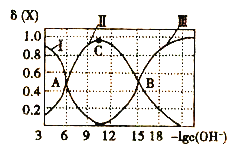
(2)�о��������¶ȡ�ѹǿ�Է�Ӧ��C6H5CH2CH3 (g)+CO2(g) ![]() C6H5CH=CH2(g)+CO(g) + H2O(g)�����ұ���ƽ��ת����Ӱ����ͼ��ʾ��
C6H5CH=CH2(g)+CO(g) + H2O(g)�����ұ���ƽ��ת����Ӱ����ͼ��ʾ��

����H_____(����>������<������ = ��)��ѹǿp1��p2��p3�Ӵ�С��˳����_____��
(3)CO�ɱ�NO2����:CO+NO2 =CO2+ NO�����¶ȸ���225��ʱ����Ӧ����![]() ��=k�� c(CO) c(NO2),
��=k�� c(CO) c(NO2), ![]() ��=k�� c(CO2) c(NO), k����k���ֱ�Ϊ�����淴Ӧ���ʳ������������¶ȷ�Χ�ڣ� k����k����÷�Ӧ��ƽ�ⳣ��K֮��Ĺ�ϵΪ___________��
��=k�� c(CO2) c(NO), k����k���ֱ�Ϊ�����淴Ӧ���ʳ������������¶ȷ�Χ�ڣ� k����k����÷�Ӧ��ƽ�ⳣ��K֮��Ĺ�ϵΪ___________��
���𰸡�(2a+b)/3 0.2mol/(L��min) 1.8 = x-2�� > p1> p2> p3 k��/k��=K
��������
�����ø�˹������Ӧ�ȣ�����������ʽ��Ϸ���ʽ���㣻������������Է�Ӧ���ʺ�ƽ�ⳣ����Ӱ�������𣻸��ݷ�Ӧ���ʱ���ʽ���ƽ�ⳣ������ʽ���
��(1)��ӦFe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)���ڷ�Ӧ�١�(2/3)����Ӧ�ڡ�(1/3)����H=��H1��(2/3)����H2��(1/3)=(2a+b)/3��
��(1)CO2ת����Ϊ75%�������ĵ�CO2�����ʵ���Ϊ8mol��75%=6mol�����Ϊ2L��ת����Ũ��Ϊ3mol��L��1����
CO2(g)+H2(g)=CO(g)+H2O(g)
��ʼ��Ũ�� 4 8 0 0
ת����Ũ�� 3 3 3 3
ƽ��ʱ��Ũ�� 1 5 3 3
��ʱΪ15min����Ӧ����![]() ��
��
ƽ�ⳣ��![]() ��
��
���������ͬ�����������������ȣ����з�Ӧ������У����ɵ�CO��H2O��ͬ�����Ҳ�����������л���������У�CO��H2O�����ʵ���������ȣ�y=z�����������ͬ�����������������ȣ�����ǰ�������ȵķ�Ӧ������Ӧ��Ҫ�ɱ������ڼ���CO2��H2�ı���Ϊ1��2�������е�CO��H2��ȫת��ΪCO2��H2������CO2�����ʵ���Ϊ��+y��H2�����ʵ���Ϊx+y��![]() ����y=x-2����
����y=x-2����
(2)��ͼ�������ߣ������¶ȵ����ߣ��ұ���ת�������ߣ�˵�������¶ȣ�ƽ�������ƶ���������ѧ�������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�������ӦΪ���ȷ�Ӧ�����H>0����ͬһ�¶��£����Է���p3ʱ���ұ���ת������ߡ��÷�ӦΪ�����������ķ�Ӧ������ѹǿ��ƽ�������������С�ķ�Ӧ�ƶ���Ϊ�淴Ӧ�����ұ���ת���ʽ��͡�˵��p3��ʾ��ѹǿ��С����õ����ϵΪp1>p2>p3��
(3)�ﵽ��ѧƽ��������Ӧ���ʵ����淴Ӧ���ʣ�![]() ��=
��=![]() ������k��c(CO)c(NO2)=k��c(CO2)c(NO)��ƽ�ⳣ��K�ı�ʾΪ
������k��c(CO)c(NO2)=k��c(CO2)c(NO)��ƽ�ⳣ��K�ı�ʾΪ![]() ��ת����ʽ��
��ת����ʽ��![]() ����k��/k��=K��
����k��/k��=K��

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�