题目内容
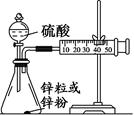
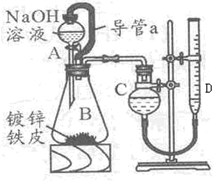
一氯甲烷,也叫甲基氯,常温下是无色气体,密度为0.9159克/厘米3,熔点为-97.73℃,沸点为-24.2℃,18℃时在水中的溶解度为280毫升/毫升水,与乙醚、丙酮或苯互溶,能溶于乙醇。在实验室里可用下图装置制取一氯甲烷:

制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸。
试填写下列空白:
(1)制备一氯甲烷的化学方程式 ,
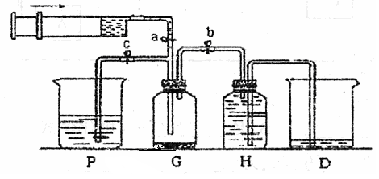
(2)装置b的作用是 ;
(3)已知卤代烃能发生碱性水解,转化为醇。装置e中可能发生的反应方程式为
;
(4)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃燃烧现象有明显区别)。CH3Cl燃烧的化学方程式是 ;
(5)实验中实际按甲醇和浓盐酸1︰2(物质量之比)进行反应的理由是 ;
(6)某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇~浓盐酸的混和液的量比正常情况下多(装置的气密性没有问题),其原因是 ;
(7)实验结束后,d中收集到的液体中含有 。

制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸。
试填写下列空白:
(1)制备一氯甲烷的化学方程式 ,
(2)装置b的作用是 ;
(3)已知卤代烃能发生碱性水解,转化为醇。装置e中可能发生的反应方程式为
;
(4)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃燃烧现象有明显区别)。CH3Cl燃烧的化学方程式是 ;
(5)实验中实际按甲醇和浓盐酸1︰2(物质量之比)进行反应的理由是 ;
(6)某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇~浓盐酸的混和液的量比正常情况下多(装置的气密性没有问题),其原因是 ;
(7)实验结束后,d中收集到的液体中含有 。
(1)CH3OH+HCl CH3Cl+H2O
CH3Cl+H2O
(2)防止倒吸,保证安全 (3)NaOH+HCl=NaCl+H2O
(4)2CH3Cl+3O2 2CO2+2H2O+2HCl
2CO2+2H2O+2HCl
(5)可使甲醇充分反应,转化成一氯甲烷
(6)甲醇沸点较低(64.7℃),受热时易挥发,致使一部分未反应而逸出
(7)甲醇、盐酸、一氯甲烷
 CH3Cl+H2O
CH3Cl+H2O (2)防止倒吸,保证安全 (3)NaOH+HCl=NaCl+H2O
(4)2CH3Cl+3O2
 2CO2+2H2O+2HCl
2CO2+2H2O+2HCl (5)可使甲醇充分反应,转化成一氯甲烷
(6)甲醇沸点较低(64.7℃),受热时易挥发,致使一部分未反应而逸出
(7)甲醇、盐酸、一氯甲烷
试题分析:(1)在催化剂的作用下,甲醇和氯化氢发生取代反应生成一氯甲烷,反应的化学方程式使CH3OH+HCl
 CH3Cl+H2O。
CH3Cl+H2O。(2)由于氯化氢极易挥发,而氯化氢又极易溶解在水中,所以装置b的作用是防止倒吸,保证安全。
(3)卤代烃能发生碱性水解,转化为醇。由于在生成醇的同时,还生成氯化氢,则装置e中可能发生的反应方程式为NaOH+HCl=NaCl+H2O。
(4)根据一氯甲烷的组成元素可知,一氯甲烷燃烧的生成物应该是CO2、水和氯化氢,则CH3Cl燃烧的化学方程式是2CH3Cl+3O2
 2CO2+2H2O+2HCl。
2CO2+2H2O+2HCl。(5)实验中实际按甲醇和浓盐酸1︰2(物质量之比)进行反应,显然盐酸是过量的,因此可以提高甲醇的转化率,使甲醇充分反应,转化成一氯甲烷。
(6)根据已知条件可知,甲醇沸点较低(64.7℃),受热时易挥发,致使一部分未反应而逸出,所以收集到一定体积的气体产物所消耗的甲醇~浓盐酸的混和液的量比正常情况下多。
(7)由于甲醇和盐酸都是易挥发的,因此实验结束后,d中收集到的液体中含有甲醇、盐酸、一氯甲烷。
点评:该题是高考中的常见题型,属于中等难度的试题。该题综合性强,侧重对学生实验能力的培养,提高学生的学科素养。有利于培养学生规范、严谨的实验设计、评价能力以及操作动手能力。该题需要明确的这种类型的试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目