题目内容
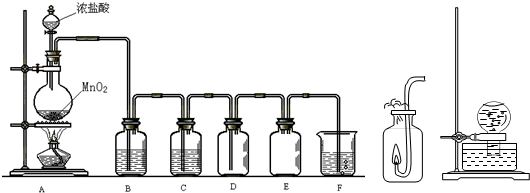
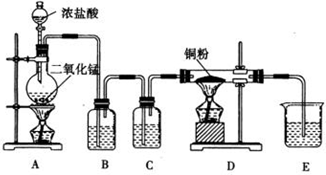
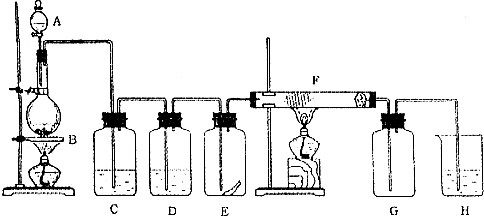
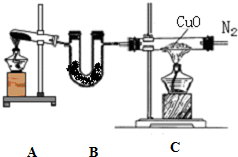
按教材中所给的装置和药品,进行实验室制取Cl2.请回答下列问题:
①对反应混合液加热时,需要“缓缓”加热,其作用是______;
②向用向上排空气法收集所得到的氯气中,加入一小块干燥的有色布条,发现有色布条慢慢褪色,试解释布条褪色的原因.______;
③多余的氯气应用______吸收,反应的离子方程式为______.
①对反应混合液加热时,需要“缓缓”加热,其作用是______;
②向用向上排空气法收集所得到的氯气中,加入一小块干燥的有色布条,发现有色布条慢慢褪色,试解释布条褪色的原因.______;
③多余的氯气应用______吸收,反应的离子方程式为______.
①对反应混合液加热时,需要“缓缓”加热,其作用是减少浓盐酸的挥发,故答案为:减少浓盐酸的挥发;
②干燥的氯气和干燥的有色布条相遇不能褪色,氯气无漂白作用,氯气遇到干燥有色布条褪色证明氯气中含有水蒸气,氯气和水反应生成的次氯酸具有漂白作用,能使干燥的有色布条褪色,
故答案为:因为这样收集的氯气不干燥,里面混有水蒸气,会产生次氯酸,所以能使干燥的有色布条褪色;
③氯气是有毒气体,污染空气不能排放到空气中,需要用氢氧化钠溶液吸收,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:NaOH溶液;Cl2+2OH-=Cl-+ClO-+H2O.
②干燥的氯气和干燥的有色布条相遇不能褪色,氯气无漂白作用,氯气遇到干燥有色布条褪色证明氯气中含有水蒸气,氯气和水反应生成的次氯酸具有漂白作用,能使干燥的有色布条褪色,
故答案为:因为这样收集的氯气不干燥,里面混有水蒸气,会产生次氯酸,所以能使干燥的有色布条褪色;
③氯气是有毒气体,污染空气不能排放到空气中,需要用氢氧化钠溶液吸收,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:NaOH溶液;Cl2+2OH-=Cl-+ClO-+H2O.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目