题目内容
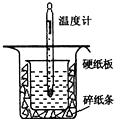
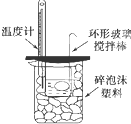
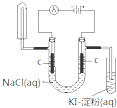
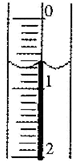
实验室用50mL0.50mol?L-1盐酸、50mL0.55mol?L-1NaOH,利用如图装置进行中和热的测定,请回答下列问题:
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是______.
(2)如用0.50mol?L-1盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将______(填“偏大”、“偏小”、“不变”)
(3)实验得到表中的数据:
经数据处理,t2-t1=3.4℃.则该实验测得的中和热△H=______
[盐酸和NaOH溶液的密度按1g?cm-3计算,反应后混合溶液的比热容(c)按4.18J?(g?℃)-1计算].

(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是______.
(2)如用0.50mol?L-1盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将______(填“偏大”、“偏小”、“不变”)
(3)实验得到表中的数据:
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
[盐酸和NaOH溶液的密度按1g?cm-3计算,反应后混合溶液的比热容(c)按4.18J?(g?℃)-1计算].

(1)不能将环形玻璃搅拌棒改为铜丝搅拌棒,因为铜丝搅拌棒是热的良导体,
故答案为:Cu传热快,热量损失大;
(2)氢氧化钠固体溶于水放热,溶液温度升高,所以实验中测得的“中和热”数值将偏大,
故答案为:偏大;
(3)50mL 0.50mol?L-1盐酸、50mL 0.55mol?L-1 NaOH的质量和为m=100mL×1g/mL=100g,c=4.18J/(g?℃),△T=t2-t1=3.4℃,代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g?℃)×100g×3.4℃=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为
=56.8kJ,即该实验测得的中和热△H=-56.8kJ/mol,
故答案为:-56.8kJ/mol.
故答案为:Cu传热快,热量损失大;
(2)氢氧化钠固体溶于水放热,溶液温度升高,所以实验中测得的“中和热”数值将偏大,
故答案为:偏大;
(3)50mL 0.50mol?L-1盐酸、50mL 0.55mol?L-1 NaOH的质量和为m=100mL×1g/mL=100g,c=4.18J/(g?℃),△T=t2-t1=3.4℃,代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g?℃)×100g×3.4℃=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为
| 1.4212KJ×1mol |
| 0.025mol |
故答案为:-56.8kJ/mol.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目