题目内容
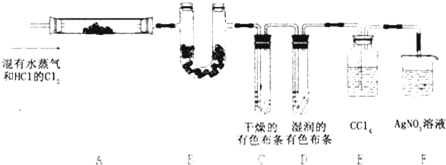
 某校化学实验兴趣小组为“证明某水煤气中CO2、CO、H2、H2O(气)共同存在”.经讨论从如下图所示提供的仪器和药品中设计组合成一套装置(假设其他杂质气体对本实验无干扰).
某校化学实验兴趣小组为“证明某水煤气中CO2、CO、H2、H2O(气)共同存在”.经讨论从如下图所示提供的仪器和药品中设计组合成一套装置(假设其他杂质气体对本实验无干扰).(1)该小组证明CO2存在应选用
C
C
装置,现象是石灰水)变浑浊
石灰水)变浑浊
.证明H2O气的存在应选用F
F
装置,现象是(无水硫酸铜)由白色变蓝色
(无水硫酸铜)由白色变蓝色
.(2)若某些仪器可重复使用,某些仪器可不使用,B中反应完全进行,连接的玻璃导管、胶管忽略.按气流从左到右,用上述字母把各装置连接组合起来,正确的连接次序是:
混合气体-
F
F
-C
C
-(B)-A
A
-F
F
-C
C
(3)此实验的操作步骤中还有一欠缺之处,应如何改进?
尾气中可能含CO而没有处理,将尾气通过导管引出用酒精灯火焰将CO燃烧掉
尾气中可能含CO而没有处理,将尾气通过导管引出用酒精灯火焰将CO燃烧掉
.分析:(1)二氧化碳能使澄清石灰水变浑浊,水能使无水硫酸铜变蓝;
(2)由于检验其他气体会引入水蒸汽,故应先检验水的存在,选用无水硫酸铜来检验,检验二氧化碳可用澄清石灰水,
除去二氧化碳和水需用碱石灰,然后气体通过灼热的氧化铜通过产物来检验一氧化碳和氢气,故可确定连接顺序.
(3)一氧化碳是有毒的气体,使用后必须进行尾气处理.
(2)由于检验其他气体会引入水蒸汽,故应先检验水的存在,选用无水硫酸铜来检验,检验二氧化碳可用澄清石灰水,
除去二氧化碳和水需用碱石灰,然后气体通过灼热的氧化铜通过产物来检验一氧化碳和氢气,故可确定连接顺序.
(3)一氧化碳是有毒的气体,使用后必须进行尾气处理.
解答:解:(1)二氧化碳能使澄清石灰水变浑浊,水能使无水硫酸铜变蓝,故检验二氧化碳选用C装置,检验水蒸汽用F装置.
故答案为:C;(石灰水)变浑浊;F;(无水硫酸铜)由白色变蓝色;
(2)由于检验其他气体会引入水蒸汽,故应先检验水的存在,选用无水硫酸铜来检验,故选用F装置;检验二氧化碳可用澄清石灰水,
选用C装置;除去二氧化碳和水需用碱石灰,选用B装置;然后气体通过灼热的氧化铜选用A装置;通过产物来检验一氧化碳和氢气,
先检验氢气后检验二氧化碳,故先连F后连C装置,所以连接顺序为:F-C-B-A-F-C.故答案为:F-C-B-A-F-C;
(3)一氧化碳是有毒的气体,必须进行尾气处理,以防造成空气污染,
故答案为:尾气中可能含CO而没有处理,将尾气通过导管引出用酒精灯火焰将CO燃烧掉.
故答案为:C;(石灰水)变浑浊;F;(无水硫酸铜)由白色变蓝色;
(2)由于检验其他气体会引入水蒸汽,故应先检验水的存在,选用无水硫酸铜来检验,故选用F装置;检验二氧化碳可用澄清石灰水,
选用C装置;除去二氧化碳和水需用碱石灰,选用B装置;然后气体通过灼热的氧化铜选用A装置;通过产物来检验一氧化碳和氢气,
先检验氢气后检验二氧化碳,故先连F后连C装置,所以连接顺序为:F-C-B-A-F-C.故答案为:F-C-B-A-F-C;
(3)一氧化碳是有毒的气体,必须进行尾气处理,以防造成空气污染,
故答案为:尾气中可能含CO而没有处理,将尾气通过导管引出用酒精灯火焰将CO燃烧掉.
点评:本题考查了常见气体的检验,完成此题,可以依据气体的性质进行,需要注意的是当检验二氧化碳和水时需要先检验水的存在,检验一氧化碳和氢气时需要先除去二氧化碳和水.

练习册系列答案
相关题目
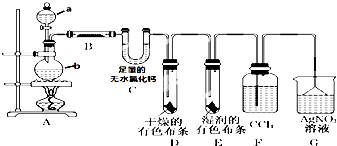 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称