题目内容
18.反应A(s)=D(g)+E(g),已知△G=△H-T△S=(-4500+11T)J/mol;要防止该反应发生,温度必须( )| A. | 低于136K | B. | 高于409K | ||
| C. | 高于136K而低于409K | D. | 低于409K |
分析 依据反应是否自发进行的判断依据是△H-T△S<0,反应自发进行,△H-T△S>0,反应不能自发进行.
解答 解:已知反应A═D+E△H-T△S=(-4 500+11T ) J•mol-1,(温度单位为K).要防止A分解反应发生,需要△H-T△S=(-4 500+11T ) J•mol-1≥0,计算得到:T≥409K
故选:B.
点评 本题考查了反应自发进行的判断依据的计算应用,注意单位的统一,题目较简单.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
9.下列热化学方程式或离子方程式中,正确的是( )
| A. | 甲烷的燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g)+3H2(g)$?_{500℃、30MPa}^{催化剂}$ 2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 硫酸与氢氧化钡发生中和反应的热化学方程式为:H+(aq)+SO42-(aq)+Ba2+(aq)+OH-(aq)=BaSO4(s)+H2O(l)△H=-57.3kJ•mol-1 | |
| D. | 氯化镁溶液与氨水反应:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+ |
6.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下,0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 标准状况下,5.6L CCl4含有的分子数为0.25 NA | |
| C. | 在标准状况下,2.8g N2和2.24LCO所含质子数均为1.4NA | |
| D. | 常温下,1 L pH=1的硫酸溶液中含有的H+数为0.05NA |
3.已知:在同一反应中,氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性强于还原产物的还原性.在一定条件下KClO3与I2按下式反应:2KClO3+I2═2KIO3+Cl2,下列判断正确的是( )
| A. | 该反应属于置换反应 | B. | 还原剂为KClO3,氧化剂为I2 | ||
| C. | 还原性:I2>KIO3 | D. | 氧化性:KClO3>KIO3 |
10.从2mol/L的氯化铜溶液中取出含Cl-为0.5mol的溶液,所取溶液的体积是( )
| A. | 1 L | B. | 0.5 L | C. | 0.25 L | D. | 0.125L |
12.下列电子式书写不正确的是( )
| A. | 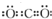 | B. | 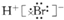 | C. | 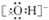 | D. | 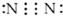 |
13.化学在生产和日常生活中有着重要的作用.下列有关说法正确的是( )
| A. | 二氧化硫有漂白性,常用作棉、麻、纸张和食品的漂白 | |
| B. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 | |
| C. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| D. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 |
