��Ŀ����
�ҹ��Ǹ��������,��������Ϊ�����һ,��¯��������Ϊ�ձ������������
I.��֪��Ӧ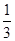 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
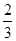 Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ�������,1000��ʱ����Fe��Fe2O3��CO��CO2��1. 0mol,��Ӧ����l0min��ﵽƽ�⡣
��1��CO��ƽ��ת����=____________
��2�������CO��ƽ��ת����,�ٽ�Fe2O3��ת��,�ɲ�ȡ�Ĵ�ʩ��________
a����߷�Ӧ�¶�
b������Ӧ��ϵ��ѹǿ
c��ѡȡ���ʵĴ���
d����ʱ���ջ��Ƴ�����CO2
e�������ʯ,ʹ����ƽ���������ֽӴ�
��.��¯���������ķ����е�CO�ɽ��л���,ʹ����һ�������º�H2��Ӧ�Ʊ��״�:
CO(g)+ 2H2(g) CH3OH(g)�������ͼʾ�ش���������:
CH3OH(g)�������ͼʾ�ش���������:
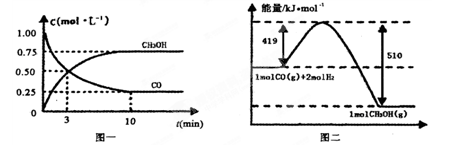
��1���ӷ�Ӧ��ʼ��ƽ��,��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)=________
��2�������¶Ⱥ�������ͬ�������ܱ�������,����ͬ��ʽͶ�뷴Ӧ��,��÷�Ӧ�ﵽƽ�ⅼ���й��������±���
�����й�ϵ��ȷ����________
A��c1=c2 B��2Q1=Q3 C��2��1=��3 D����1+��2 =1
E���÷�Ӧ������1mol CH3OH����ų�(Q1+Q2)kJ����
���Լ���Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺
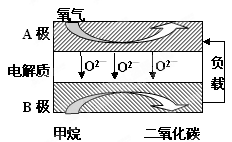
��1��B���ϵĵ缫��ӦʽΪ
��2�����ø�ȼ�ϵ������Դ����ʯī���缫���100mL 1mol/L������ͭ��Һ���������ռ���������������ʱ�����������ĵļ�������Ϊ ������£���
I.��֪��Ӧ
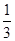 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
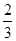 Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ�������,1000��ʱ����Fe��Fe2O3��CO��CO2��1. 0mol,��Ӧ����l0min��ﵽƽ�⡣
��1��CO��ƽ��ת����=____________
��2�������CO��ƽ��ת����,�ٽ�Fe2O3��ת��,�ɲ�ȡ�Ĵ�ʩ��________
a����߷�Ӧ�¶�
b������Ӧ��ϵ��ѹǿ
c��ѡȡ���ʵĴ���
d����ʱ���ջ��Ƴ�����CO2
e�������ʯ,ʹ����ƽ���������ֽӴ�
��.��¯���������ķ����е�CO�ɽ��л���,ʹ����һ�������º�H2��Ӧ�Ʊ��״�:
CO(g)+ 2H2(g)
 CH3OH(g)�������ͼʾ�ش���������:
CH3OH(g)�������ͼʾ�ش���������:
��1���ӷ�Ӧ��ʼ��ƽ��,��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)=________
��2�������¶Ⱥ�������ͬ�������ܱ�������,����ͬ��ʽͶ�뷴Ӧ��,��÷�Ӧ�ﵽƽ�ⅼ���й��������±���
| ���� | ��Ӧ��Ͷ����� | ��Ӧ��� ת���� | CH3OH��Ũ�� | �����仯 (Q1��Q2��Q3������0) |
| �� | 1mol CO��2mol H2 | ��1 | c1 | �ų�Q1kJ���� |
| �� | 1mol CH3OH | ��2 | c2 | ����Q2kJ���� |
| �� | 2mol CO��4mol H2 | ��3 | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ����________
A��c1=c2 B��2Q1=Q3 C��2��1=��3 D����1+��2 =1
E���÷�Ӧ������1mol CH3OH����ų�(Q1+Q2)kJ����
���Լ���Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺

��1��B���ϵĵ缫��ӦʽΪ
��2�����ø�ȼ�ϵ������Դ����ʯī���缫���100mL 1mol/L������ͭ��Һ���������ռ���������������ʱ�����������ĵļ�������Ϊ ������£���
I����1��60����2�֣� ��2��d��2�֣�
��1��0.15mol/(L��min) ��2�֣�����λ������1�֣�
��2�� A D E (3�֣��д�ѡ���÷�)
��1�� CH4 + 4O2�� ��8e��= CO2+ 2H2O����2�֣�
��2�� 1.12 L��2�֣�
��1��0.15mol/(L��min) ��2�֣�����λ������1�֣�
��2�� A D E (3�֣��д�ѡ���÷�)
��1�� CH4 + 4O2�� ��8e��= CO2+ 2H2O����2�֣�
��2�� 1.12 L��2�֣�
���������I.��1����ƽ��ʱCO�����ʵ����仯Ϊnmol����
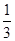 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
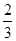 Fe(s)+ CO2(g)
Fe(s)+ CO2(g) ��ʼ��mol����1 1
�仯��mol����n n
ƽ�⣨mol����1-n n+1
����n+1/(1-n)=4�����n=0.6����CO��ƽ��ת����Ϊ0.6mol/1mol��100%=60%���ʴ�Ϊ��60%�� (2)a���÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ����߷�Ӧ�¶ȣ�ƽ�����淴Ӧ�ƶ���CO��ƽ��ת���ʽ��ͣ���a����b����Ӧǰ����������ʵ������䣬��С�������ݻ�������ѹǿƽ�ⲻ�ƶ���CO��ƽ��ת���ʲ��䣬��b����c��������ʵĴ�����ƽ�ⲻ�ƶ�����c����d���Ƴ�����CO2��ƽ��������Ӧ�ƶ���CO��ƽ��ת��������d��ȷ��e�������ʯ��ʹ����ƽ���������ֽӴ���ƽ�ⲻ�ƶ�����e����ѡd�� III��1���ﵽƽ��ʱ���ɼ״�Ϊ��0.75mol/L�������ĵ�c��H2��=2��0.75mol/L=1.5mol/L��v��H2��=��c/��t=1.5mol/L/10min=0.15mol/��L min����2��A���ס�����Ƚϣ����ҵ�ЧΪ��ʼ����1mol CO��2mol H2���ͼ��ǵ�Ч�ģ������ǵ�Чƽ�⣬����ƽ��ʱ�״���Ũ��c1=c2����A��ȷ��B���ס�����Ƚϣ����з�Ӧ������ʵ���Ϊ��2����ѹǿ�����ڷ�ӦCO��g��+2H2��g�� CH3OH��g����ƽ�������ɼ״��ķ����ƶ�����2Q1��Q3����B����C���ס�����Ƚϣ����з�Ӧ������ʵ���Ϊ��2����ѹǿ�����ڷ�ӦCO��g��+2H2��g��=CH3OH��g����ƽ�������ɼ״��ķ����ƶ�����a1��a3 ����C����D���ס��Ҵ�����ͬ��ƽ��״̬�����ҷ�Ӧ�����෴�����1+��2="1" ,��D��ȷ��E���ס��Ҵ�����ͬ��ƽ��״̬�����ҷ�Ӧ�����෴����������ת���ĺ�ǡ��Ϊ1mol�����Ը÷�Ӧ������1mol CH3OH����ų���Q1+Q2��kJ��������E��ȷ���ʴ�Ϊ��ADE����1��ͨ��ȼ�ϼ���ĵ缫�Ǹ�����ͨ�������ĵ缫�����������������ĵ缫ʽΪCH4 + 4O2����8e��= CO2+ 2H2O����2���������ͭ��Һʱ�����ĵ缫��Ӧʽ4OH�� ��4e��= O2��+ 2H2O�������ķ�Ӧʽ�ǣ� Cu2++2e-=Cu��2H++e-=H2����N(Cu)=0.1mol.�������ռ��������������ȣ��������ʵ���ΪX����4X=0.1��2+2X�����X=0.1.��������Ӧ����ת�Ƶ�����ȡ����ӵ����ʵ���Ϊ0.4mol.����ÿĦ������ʧȥ����8Ħ����������Ҫ��������ʵ���Ϊ0.05Ħ����V��CH4��=0.05Ħ����22.4��/Ħ��=1.12 �� ��ʵ�������ĵļ�������������ϴ���ԭ���Ǽ��鲻��ȫ������������C��CO �� �������ת���ʴﲻ��100%��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ


 Fe3��(aq)��3OH��(aq) ��H��a kJ/mol
Fe3��(aq)��3OH��(aq) ��H��a kJ/mol
 CO(NH2)2(l)��H2O(g)��
CO(NH2)2(l)��H2O(g)�� C H4 (g)+2 H2O(g)����һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2 0.2 mol��Lһ1��H2 0.8 mol��Lһ1��CH40.8 mol��Lһ1��H2O1.6 mol��Lһ1����CO2��ƽ��ת����Ϊ________��300 ��ʱ������Ӧ��ƽ�ⳣ��K=____________________��200��ʱ�÷�Ӧ��ƽ�ⳣ��K=64.8����÷�Ӧ�ġ�H_____(���������<��)O��
C H4 (g)+2 H2O(g)����һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2 0.2 mol��Lһ1��H2 0.8 mol��Lһ1��CH40.8 mol��Lһ1��H2O1.6 mol��Lһ1����CO2��ƽ��ת����Ϊ________��300 ��ʱ������Ӧ��ƽ�ⳣ��K=____________________��200��ʱ�÷�Ӧ��ƽ�ⳣ��K=64.8����÷�Ӧ�ġ�H_____(���������<��)O��



 ��
��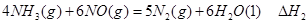 ��
�� ��
�� ��
�� ��
�� ����֮���ϵ�ı���ʽ��
����֮���ϵ�ı���ʽ��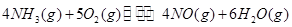
 ��
��






