题目内容
8.相对分子质量为142的脂环化合物M在氧气中燃烧只生成二氧化碳和水,M中含有一个六元环和氢氧化钠溶液反应生成两种有机产物.M不能与碳酸氢钠反应,则M分子环上一氯代物同分异构体有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 脂环化合物中的环是由C原子相互连接形成的,则M中含有一个六元环,该六元环是由6个C原子形成的;M能够与氢氧化钠溶液反应,则M分子中含有酯基,据此可判断M分子中含有至少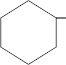 和酯基(-COOC-)结构,再结合其相对分子质量为142确定其分子组成及结构简式,最后根据M分子环上的等效H原子数判断其一氯代物的同分异构体数目.
和酯基(-COOC-)结构,再结合其相对分子质量为142确定其分子组成及结构简式,最后根据M分子环上的等效H原子数判断其一氯代物的同分异构体数目.
解答 解:M中含有一个六元环和氢氧化钠溶液反应生成两种有机产物,则M分子中含有酯基和6个C原子形成的碳环;M不能与碳酸氢钠反应,则M分子中不含羧基;有机物M完全燃烧后只生成二氧化碳和水,说明没有C、H、O以外的元素,
根据分析可知,M分子中含有至少 和酯基(-COOC-)结构,即:M分子中至少含有8个C、2个O原子,总原子量为:12×8+16×2=128,剩余的相对原子量为:142-128=14,只能含有14个H原子,
和酯基(-COOC-)结构,即:M分子中至少含有8个C、2个O原子,总原子量为:12×8+16×2=128,剩余的相对原子量为:142-128=14,只能含有14个H原子,
所以M的结构简式为: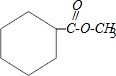 ,其分子环上含有4种等效H,则M分子环上一氯代物同分异构体有4种,
,其分子环上含有4种等效H,则M分子环上一氯代物同分异构体有4种,
故选C.
点评 本题考查了同分异构体数目的求算,题目难度中等,根据题干信息推断出M的结构简式为解答关键,注意明确脂环化合物的含义,还要注意“M分子环上”的一氯代物,为易错点.

练习册系列答案
相关题目
13.某有机物在氧气里充分燃烧,生成CO2和H2O的质量比为22:9,由此可得出的正确的结论是( )
| A. | 碳、氢、氧的原子个数比为1:2:3 | |
| B. | 碳、氢的原子个数比为1:1 | |
| C. | 该有机物中肯定不含氧元素 | |
| D. | 不能判断该有机物中是否含有氧元素 |
13.已知某脂肪酸(用R表示)有以下实验记录:
则以下关于R的结论肯定不正确的是( )
| 组成元素 | 官能团 | 相对分子质量 | 与碱反应 | 加成反应 |
| C、H、O | 羧基、碳碳双键 | 小于300 | 14.0gR可被2.0gNaOH中和 | 2.8gR可与448mLH2(标准状况)反应 |
| A. | R是一元羧酸 | B. | R分子在烃基为C17H${\;}_{3{1}^{-}}$ | ||
| C. | R的相对分子质量为280 | D. | R分子含一个碳碳双键 |

 某研究性学习小组的同学通过对亚硫酸钠组成元素的价态进行分析后认为Na2SO3溶液在存放过程中有可能变质,若已变质,则相应反应的化学方程式2Na2SO3+O2=2Na2SO4.
某研究性学习小组的同学通过对亚硫酸钠组成元素的价态进行分析后认为Na2SO3溶液在存放过程中有可能变质,若已变质,则相应反应的化学方程式2Na2SO3+O2=2Na2SO4.

 (R、R′表示烃基或氢)
(R、R′表示烃基或氢) ,E的结构简式是CH3CHO.
,E的结构简式是CH3CHO.
 .
.