题目内容
13.食品添加剂硫酸铝铵[NH4Al(SO4)2]可作煮、炖食品的护色剂.组成该化合物的各原子中,原子半径最大的是( )| A. | N | B. | S | C. | Al | D. | O |
分析 所以元素中H原子半径最小,同周期随原子序数增大原子半径减小,一般电子层越多原子半径越大.
解答 解:所以元素中H原子半径最小,同周期随原子序数增大原子半径减小,一般电子层越多原子半径越大,故原子半径:Al>S>N>O>H,故选C.
点评 本题考查原子半径比较,注意对元素周期律的理解掌握,侧重对基础知识的巩固.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
4.如图是元素周期表的一部分.
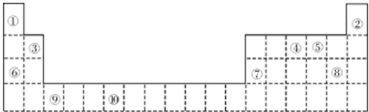
(1)元素⑤的未成电子数为2.
(2)如果在温度接近373K时,根据M=mn测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是分子间存在氢键,H2O分子发生缔合
(3)要证明太阳上是否含有②元素,可采用的方法是光谱分析.
(4)某些不同族元素的性质也有一定的相似性,加上表中元素⑦与元素③的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的离子方程式2OH-+Be(OH)2=BeO22-+2H2O.
(5)根据下列五种元素的第一至第四电力能数(单位:kJ•mol-1).回答下面各题:
(Ⅰ)在周期表中,最可能处于同一主族的是R和U(填匀速代号)
(Ⅱ)T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素,位于IIIA族;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.
(6)⑩元素M能形成化合物(MO2Cl2).请回答下列问题:
(Ⅰ)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有K、Cu(填元素符号)
(Ⅱ)MO2Cl2常温下为深红色液体,能与CCl2、CS2等互溶,据此可判断MO2Cl2是非极性(填“极性”或“非极性”)分子.

(1)元素⑤的未成电子数为2.
(2)如果在温度接近373K时,根据M=mn测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是分子间存在氢键,H2O分子发生缔合
(3)要证明太阳上是否含有②元素,可采用的方法是光谱分析.
(4)某些不同族元素的性质也有一定的相似性,加上表中元素⑦与元素③的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的离子方程式2OH-+Be(OH)2=BeO22-+2H2O.
(5)根据下列五种元素的第一至第四电力能数(单位:kJ•mol-1).回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
(Ⅱ)T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素,位于IIIA族;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.
(6)⑩元素M能形成化合物(MO2Cl2).请回答下列问题:
(Ⅰ)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有K、Cu(填元素符号)
(Ⅱ)MO2Cl2常温下为深红色液体,能与CCl2、CS2等互溶,据此可判断MO2Cl2是非极性(填“极性”或“非极性”)分子.
1.下列说法不正确的是( )
| A. | 已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol. CO(g)+12O2(g)═CO2(g),△H=-283.0 kJ/mol. C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol. 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol | |
| C. | 实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 | |
| D. | 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=(cα)2c(1−α).若加入少量醋酸钠固体,则CH3COOH?CH3COO-+H+向左移动,α减小,Ka变小 |
8. 节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务.下列举措不符合这一要求的是( )
节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务.下列举措不符合这一要求的是( )
 节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务.下列举措不符合这一要求的是( )
节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务.下列举措不符合这一要求的是( )| A. | 倡导开私家车的人乘公交车上下班 | |
| B. | 用节能灯代替白炽灯 | |
| C. | 政府鼓励科研和生产部门开发、利用太阳能 | |
| D. | 加快开发石油以缓解能源紧张问题 |
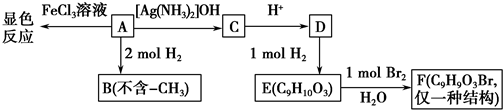
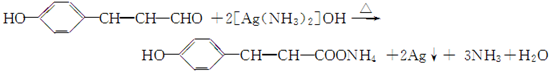 .
. .
. ,G的结构简式为:
,G的结构简式为: .
. .
. 或
或 (写出一个反应方程式即可).
(写出一个反应方程式即可). .
. .
. .
.

 请完成填空:
请完成填空: .
. .
.