题目内容
6.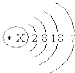 已知溴原子的原子结构示意图如图﹕
已知溴原子的原子结构示意图如图﹕(1)溴原子的原子的序数为35.
(2)溴元素的原子在反应中易得到1个电子,表现为氧化性性(填氧化性或还原性);
(3)溴元素的最高化合价+7,最低化合价-1.
(4)溴元素的非金属性比氯元素的非金属性弱(填“强”或“弱”).
(5)写出氯元素,溴元素最高价氧化物对应的水化物的化学式并比较他们的酸性强弱HClO4>HBrO4.
分析 (1)核外电子数之和等于原子序数;
(2)最外层7个电子,易得到1个电子形成最外层8电子稳定结构;
(3)最外层电子数=最高化合价数,最低化合价=最高化合价数-8;
(4)Cl、Br同主族,原子序数大的非金属性弱;
(5)Cl的非金属性强,非金属性越强,最高价氧化物对应的水化物的酸性越强.
解答 解:(1)核外电子数之和等于原子序数,则原子序数为2+8+18+7=35,故答案为:35;
(2)最外层7个电子,易得到1个电子形成最外层8电子稳定结构,表现其氧化性,故答案为:1;氧化性;
(3)最外层电子数=最高化合价数=+7,最低化合价=最高化合价数-8=7-8=-1,故答案为:+7;-1;
(4)Cl、Br同主族,原子序数大的非金属性弱,则溴元素的非金属性比氯元素的非金属性弱,故答案为:弱;
(5)Cl的非金属性强,非金属性越强,最高价氧化物对应的水化物的酸性越强,则酸性为HClO4>HBrO4,故答案为:HClO4>HBrO4.
点评 本题考查卤素元素的原子结构及元素化合物性质,为高频考点,把握原子结构与元素的性质、元素周期律等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
16.某化学式为C3H6O2的有机物的PMR谱有三个信号蜂,其强度比为3:2:1,则该有机物的结构简式不可能是( )
| A. | CH3CH2COOH | B. | CH3COOCH3 | C. | HCOOCH2CH3 | D. | CH3COCH2OH |
17.已知aXn+和bYm-的电子层结构相同,则下列关系式正确的是( )
| A. | a=b+m+n | B. | a=b-m+n | C. | a=b+m-n | D. | a=b-m-n |
14.对于H3O+的下列说法中正确的是( )
| A. | O原子采用SP2杂化 | B. | O原子采用SP3杂化 | ||
| C. | 离子中不存在配位键 | D. | 离子中存在非极性键 |
1.能证明SO2中混有CO2的方法是( )
| A. | 通过品红溶液 | |
| B. | 通过澄清石灰水 | |
| C. | 先通过高锰酸钾溶液,再通过澄清石灰水 | |
| D. | 先通过澄清石灰水,再通过高锰酸钾溶液 |
11.下列反应中原子利用率高,符合“绿色化学”要求,无污染环境因素的是( )
| A. | 乙烷与Cl2反应制氯乙烷 | B. | 乙醇和浓硫酸共热制乙烯 | ||
| C. | 乙酸和乙醇共热酯化 | D. | 乙烯与氧气在银催化作用下生成 |
18.一氧化碳、烯烃和氢气在催化剂作用下发生烯烃的醛化反应,如由乙烯可制丙醛:
CH2═CH2+CO+H2催化剂→CH3CH2CHO
由丙烯进行醛化反应也可得到醛,下列说法正确的是( )
CH2═CH2+CO+H2催化剂→CH3CH2CHO
由丙烯进行醛化反应也可得到醛,下列说法正确的是( )
| A. | 能得到一种醛 | B. | 能得到二种醛 | ||
| C. | 能得到三种醛 | D. | 该反应为取代反应 |
16.下列化合物中同分异构体数目(其中芳香族化合物的同分异构体要仍未芳香族化合物)最多的是( )
| A. | 丁烯 | B. | 乙苯 | C. | 苯甲醇 | D. | 丙酸甲酯 |
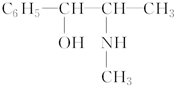
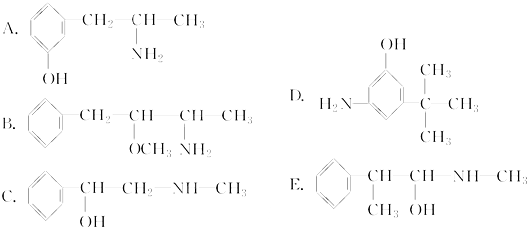
 ;
;