题目内容
8.有短周期的aXn+、bYm- 两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )| A. | b-a=n+m | B. | a-b=n+m | C. | 核电荷数X>Y | D. | 质子数Y>X |
分析 有短周期的aXn+、bYm- 两种元素的简单离子,若它们的电子层结构相同,即二者的核外电子数相等,存在a-n=b+m,离子核电荷数=原子序数=核内质子数,阳离子在阴离子的下一周期,据此分析解答.
解答 解:有短周期的aXn+、bYm- 两种元素的简单离子,若它们的电子层结构相同,即二者的核外电子数相等,存在a-n=b+m,离子核电荷数=原子序数=核内质子数,阳离子在阴离子的下一周期,
A.根据以上分析知,b-a=-(m+n),故A错误;
B.根据以上分析知,a-b=m+n,故B正确;
C.离子核电荷数=质子数,所以X的核电荷数是a、Y的核电荷数是b,阳离子在阴离子的下一周期,所以核电荷数X>Y,故C正确;
D.X的质子数是a、Y的质子数是b,阳离子在阴离子的下一周期,所以质子数X>Y,故D错误;
故选BC.
点评 本题考查元素周期表结构和应用,明确元素周期表结构、原子结构是解本题关键,知道质子数、核电荷数、电子数、电荷数之间的关系,题目难度不大.

练习册系列答案
相关题目
17.煤矸石是采煤和洗煤时的废弃物,其主要成分是Al2O3、SiO2,另外还含有数量不等的Fe2O3、CaO、MgO、Na2O、K2O、P2O5、SO3和微量稀有元素(如Ga等).下列关于煤矸石的说法正确的是( )
| A. | 可用于生产矸石水泥、耐火砖等建筑材料 | |
| B. | 煤矸石中的金属氧化物均为碱性氧化物 | |
| C. | P2O5和SO3对应水化物的酸性较强的是 H3PO4 | |
| D. | 铝比镓活泼,能电解GaCl3水溶液制备镓单质 |
18.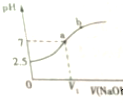 常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )
常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )
 常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )
常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )| A. | NaHSO3溶液呈酸性 | B. | V1<10mL | ||
| C. | 在a点,c(Na+)=c(SO32- )+c(HSO3-) | D. | HSO3-的电离常数Ka=6.25×10-7 |
16.亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量,某兴趣小组进行下面实验探究,查阅资料知道:
①2NO+Na2O2=2NaNO2②2NO2+Na2O2=2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-还原成Mn2+.
Ⅰ.产品制备与检验:用如图1装置制备NaNO2:
(1)写出装置A烧瓶中发生反应的化学方程式并标出电子转移的方向和数目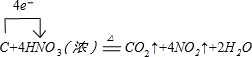 .
.
(2)B装置的作用是将NO2转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO).
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净NaNO2应在B、C装置间增加一个装置,请在右框内画出增加的装置图2,并标明盛放的试剂.
(4)试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论)取少量装置C中产物置于试管中,加入适量蒸馏水溶解,(加入稀硫酸酸化)滴加入1-2滴(少量)酸性KMnO4溶液,若溶液紫色褪去,说明C中产物含有NaNO2.
Ⅱ.含量的测定
称取装置C中反应后的固体4.000g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
(5)第一组实验数据出现异常,造成这种异常的原因可能是AC(双项选择).
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
D.滴定终了俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%或0.8625.
(结果保留4位有效数字)
①2NO+Na2O2=2NaNO2②2NO2+Na2O2=2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-还原成Mn2+.
Ⅰ.产品制备与检验:用如图1装置制备NaNO2:

(1)写出装置A烧瓶中发生反应的化学方程式并标出电子转移的方向和数目
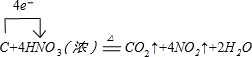 .
.(2)B装置的作用是将NO2转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO).
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净NaNO2应在B、C装置间增加一个装置,请在右框内画出增加的装置图2,并标明盛放的试剂.
(4)试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论)取少量装置C中产物置于试管中,加入适量蒸馏水溶解,(加入稀硫酸酸化)滴加入1-2滴(少量)酸性KMnO4溶液,若溶液紫色褪去,说明C中产物含有NaNO2.
Ⅱ.含量的测定
称取装置C中反应后的固体4.000g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
D.滴定终了俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%或0.8625.
(结果保留4位有效数字)
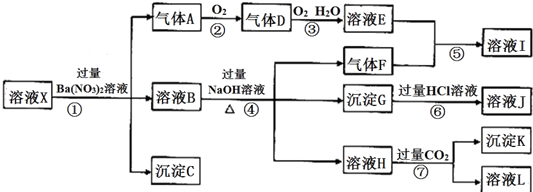
3. 已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )
已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )
 已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )
已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略).下列说法正确的是( )| A. | 若A为非金属单质,则它与Mg反应的产物,其阴阳离子个数比可能为2:3 | |
| B. | 若A为非金属单质,则其组成元素在周期表中的位置肯定处于第二周期第VA族 | |
| C. | 若D的浓溶液在常温下能使铁、铝发生钝化,则A一定为非金属单质 | |
| D. | 若A是共价化含物,0.l mol的A分子中含有的电子数可能为NA (NA为阿佛加德罗常数的值) |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 在标准状况下,2.24 L苯含有的分子数为0.1NA | |
| B. | 100ml 1mol/L的NH4Cl溶液中,NH4+的数目为0.1NA | |
| C. | 7.8 g Na2S和Na2O2的混合物中所含离子数为0.3NA | |
| D. | 电解精炼铜时,阳极质量每减少32 g,电路中就转移NA个电子 |
18.相关化学用语表示正确的是( )
| A. | NH4Br的电子式: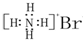 | |
| B. | S的结构示意图: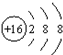 | |
| C. | 次氯酸的结构式:H-Cl-O | |
| D. | 原子核内有18个中子的氯原子:${\;}_{17}^{35}$Cl |