题目内容
用惰性电极电解100mL4mol ·L-1的CuSO4溶液,一定时间后在阳极收集到1.12 L气体,向电解后的溶液中加入足量的铁粉,充分作用后溶液中的Fe2+浓度为(设溶液的体积不变,反应前后均为标准状况)( )
| A.2.7 mol· L-1 | B.3 mol· L-1 | C.4 mol· L-1 | D.1 mol· L |
C
试题分析:惰性电极电解硫酸铜,生成物是氧气、硫酸和铜。加入铁粉后发生氧化还原反应,生成硫酸亚铁,所以根据S原子守恒可知,硫酸亚铁的物质的量浓度与原硫酸铜的物质的量浓度应该是相等的,所以反应后溶液中Fe2+浓度4 mol/L,为即答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。该题设计新颖,基础性强,再注重对学生基础知识的训练与检验的同时,侧重对学生答题能力的培养和方法指导,有利于培养学生的逻辑推理能力。该题的关键是在理解电解池原理的基础上,结合守恒法计算并能灵活运用即可。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
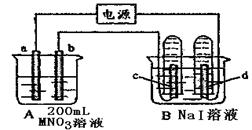
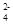 中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。
中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。