题目内容
某硫酸厂废气厂SO2的回收利用方案如下图所示,下列说法不正确的是: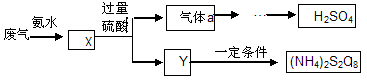
| A.X可能含有2种盐 | B.a是SO3 |
| C.Y可能含(NH4)2SO4 | D.(NH4)2S2O8中S元素的化合价不可能为+7 |
B
解析试题分析:A.将含有SO2的废气中通入氨水中,若气体少量,发生反应:SO2+2NH3+H2O=(NH4)2SO4,若气体足量,发生反应:SO2+NH3+H2O=NH4HSO4。故X可能含有2种盐。正确。B.向X中加入过量的H2SO4会发生反应产生SO2和NH4HSO4或(NH4)2SO4。SO2氧化得到SO3.SO3被浓硫酸吸收得到硫酸。因此B错误,C正确。由于S原子的最外层电子数为6个,所以在(NH4)2S2O8中S元素的化合价不可能为+7。正确。
考点:考查硫酸厂废气厂SO2的回收利用的工作原理的知识。

练习册系列答案
相关题目
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素
| A.在自然界中只以化合态的形式存在 | B.单质常用作半导体材料和光导纤维 |
| C.最高价氧化物不与酸反应 | D.气态氢化物比甲烷稳定 |
气体甲(中学常见)通入溶液乙中,随着甲的通入,溶液乙的颜色逐渐褪去,加热褪色后的溶液不再恢复原来的颜色。下列说法正确的是
| A.气体甲一定不是SO2 | B.气体甲一定是Cl2 |
| C.气体甲一定不是发生了化合反应 | D.气体甲一定被溶液乙氧化 |
已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。
实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是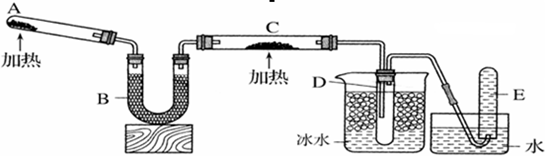
| A.反应中氧化剂和还原剂的物质的量之比为2∶3 |
| B.装置B中加入的物质可以是碱石灰或无水氯化钙 |
| C.装置D中液体可以使干燥的红色石蕊试纸变蓝 |
| D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气 |
下列关于氯水的说法正确的是
| A.向氯水中通入少量二氧化硫,氯水的漂白性增强 |
| B.氯水中加入NaCl固体,对溶液的pH无影响 |
| C.常温下,pH=2的氯水中:c(Cl-)+c(ClO-)+c(OH-)=0.01mol/L |
| D.向氯水中滴加少量NaHCO3溶液的离子反应方程式为:Cl2+2HCO3-=2CO2↑+Cl-+ClO-+H2O |
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | SO2有漂白性 | SO2能使紫色石蕊试液褪色 |
| B | 浓硫酸具有吸水性和强氧化性 | 将浓硫酸滴到用水润湿的蔗糖中,蔗糖变黑色海绵状 |
| C | 在一定条件下铁与水可以发生反应 | 将水蒸气通过灼热的铁粉,粉末变红 |
| D | 盐类水解都是吸热反应 | 向0.1mol·L-1 Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深。 |
用如图所示装置制取表格中的四种干燥、纯净的气体(必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中正确的是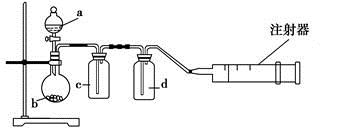
| 选项 | 气体 | a | b | c | d |
| A | SO2 | 浓硫酸 | Cu | H2O | 浓硫酸 |
| B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
| C | NH3 | 饱和NH4Cl溶液 | 消石灰 | 空集气瓶 | 固体NaOH |
| D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |
某同学利用如图所示装置进行实验,一段时间后,水沿导管缓慢上升。下列说法错误的是( )。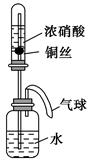
| A.实验过程中气球体积会发生变化 |
| B.广口瓶中液体的pH减小 |
| C.广口瓶中有化合反应发生 |
| D.试管中不可能发生分解反应 |
