题目内容
已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。
实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是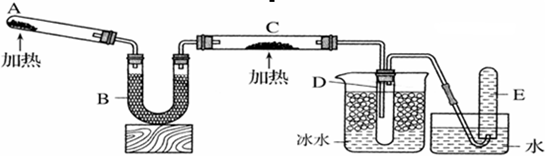
| A.反应中氧化剂和还原剂的物质的量之比为2∶3 |
| B.装置B中加入的物质可以是碱石灰或无水氯化钙 |
| C.装置D中液体可以使干燥的红色石蕊试纸变蓝 |
| D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气 |
C
解析试题分析:A.在装置A中发生反应制取氨气。通过盛有碱石灰的干燥管B干燥得到干燥的氨气。在C中发生反应:2NH3+3CuO N2+3H2O+3Cu.会看到固体由黑色变为红色。在该反应中NH3作还原剂,CuO作氧化剂,在反应中氧化剂和还原剂的物质的量之比为3∶2.错误。B.NH3是碱性气体,能用碱性干燥剂如碱石灰来干燥。但是由于氨气能与无水氯化钙发生反应得到CaCl2·8NH3.所以不能用无水氯化钙干燥。错误。C.反应产生的水被冷却为液态,未反应的氨气溶解在其中,使溶液呈碱性,所以在装置D中液体可以使干燥的红色石蕊试纸变蓝。正确。D.为防止装置D中发生倒吸,可以在DE之间安装一个安全瓶。由于氮气的密度与空气接近。所以一般不用排空气法收集氮气。错误。
N2+3H2O+3Cu.会看到固体由黑色变为红色。在该反应中NH3作还原剂,CuO作氧化剂,在反应中氧化剂和还原剂的物质的量之比为3∶2.错误。B.NH3是碱性气体,能用碱性干燥剂如碱石灰来干燥。但是由于氨气能与无水氯化钙发生反应得到CaCl2·8NH3.所以不能用无水氯化钙干燥。错误。C.反应产生的水被冷却为液态,未反应的氨气溶解在其中,使溶液呈碱性,所以在装置D中液体可以使干燥的红色石蕊试纸变蓝。正确。D.为防止装置D中发生倒吸,可以在DE之间安装一个安全瓶。由于氮气的密度与空气接近。所以一般不用排空气法收集氮气。错误。
考点:考查氨气的性质、产物的检验、气体的干燥、收集等实验基础知识。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案下列说法正确的是( )
| A.非金属元素R所形成的含氧酸盐(NaROb)中的R元素必定呈现正价 |
| B.只有非金属能形成含氧酸或含氧酸盐 |
| C.除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| D.非金属的最高价含氧酸都具有强氧化性 |
通过实验观察,某气体有下列性质:①有刺激性气味;②可使品红溶液褪色;③溶于水其水溶液可使石蕊试液变红;④通入浓硝酸中有红棕色气体产生;⑤可使溴水褪色。据此推测该气体可能是
| A.HCl | B.NH3 | C.Cl2 | D.SO2 |
某硫酸厂废气厂SO2的回收利用方案如下图所示,下列说法不正确的是: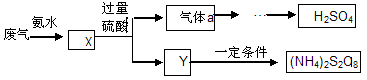
| A.X可能含有2种盐 | B.a是SO3 |
| C.Y可能含(NH4)2SO4 | D.(NH4)2S2O8中S元素的化合价不可能为+7 |
将足量的SO2通入下列各溶液中,所含离子还能大量共存的是
| A.K+、SiO32-、Cl-、NO3- |
| B.H+、NH4+、Al3+、SO42- |
| C.Na+、Cl-、MnO4-、SO42- |
| D.Na+、CO32-、CH3COO-、HCO3- |
下列叙述中正确的是
| A.实验室制取氨气的发生装置与用高锰酸钾制取氧气的装置相同 |
| B.并不是所有的铵盐都能与烧碱共热生成氨气 |
| C.除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO |
| D.CO2、NO2、P2O5均与水反应生成酸为酸性氧化物 |
已知X为一种常见酸的浓溶液,能使蔗糖变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是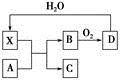
| A.X使蔗糖变黑的现象主要体现了X的脱水性 |
| B.若A为铁,则足量A与X在室温下即可完全反应 |
| C.若A为碳单质,则将C通入少量的澄清石灰水中,一定可以观察到白色沉淀产生 |
| D.工业上,B转化为D的反应条件为高温、高压、使用催化剂 |
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl—→2KCl+5Cl2↑+2MnCl2+8H2O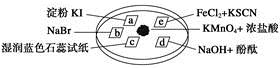
对实验现象的“解释或结论”正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |