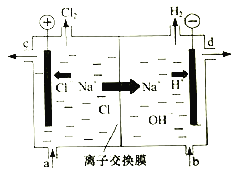
题目内容
【题目】已知A、B、D、E、F均为短周期元素(原子序数B<A<F<E<D)。25℃时,其最高价氧化物的水化物(设浓度均为0.001mol/L)溶液的pH和原子半径的关系如图所示。下列说法中正确的是

A. A和F的简单离子半径大小顺序:A < F
B. 上述五种元素中有两种元素是金属元素
C. D的最高价氧化物水化物的化学式为HDO3
D. D、E的气态氢化物的稳定性:D > E
【答案】D
【解析】
由图可知,原子半径F>E>D>B>A, F的半径最大且其0.001mol/L最高价氧化物对应的水化物溶液pH=11,则F为Na元素; 0.001mol/L A的最高价氧化物对应的水化物和0.001mol/L D的最高价氧化物对应的水化物溶液的pH=3,且原子半径D>A,则D为Cl元素,A为N元素;0.001mol/L B的高价氧化物对应的水化物溶液的3<pH<7,结合原子半径可知B为C元素。0.001mol/L E的最高价氧化物对应的水化物溶液的pH<3,则E为S元素;
A.N和Na的简单离子的电子层结构相同,N的原子序数较小,故N3-的半径大于Na+,故A项错误;
B.A、B、D、E、F 五种元素中只有F是金属元素,故B项错误;
C.D的最高价氧化物水化物的化学式为HClO4,故C项错误;
D.D、E的气态氢化物分别为H2S和HCl,的稳定性HCl>H2S ,故D项正确;
综上,本题选D。

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】25℃时,四种溶液的pH如下:
① | ② | ③ | ④ | |
pH | 3 | 3 | 11 | 11 |
溶液 | 盐酸 | 醋酸 | NaOH溶液 | 氨水 |
(1)③的溶液中由水电离出c(H+)水·c(OH-)水=______________(mol/L)2。
(2)②中加入少量醋酸钠晶体后,溶液的pH________。(填“增大”、“减小”或“不变”)
(3)②和③两溶液等体积混合,所得溶液中c(Na+)______c(CH3COO-)(填“>”、“<”或“=”)。
(4)若一定体积的①和④恰好完全反应生成氯化铵溶液,该溶液中离子浓度由大到小的顺序是_________________________________。
(5)25℃时,a mol/L醋酸溶液与b mol/LNaOH溶液等体积混合后pH=7,则醋酸的电离常数Ka=__________。(用含a、b的代数式表示)