题目内容
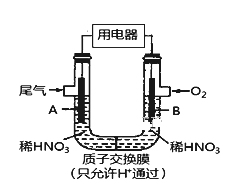
【题目】某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔导电材料。下列说法一定正确的是( )
A. 该电池工作时,电子的流向外电路由A到B,内电路由B到A形成闭合回路
B. 电极B附近的HNO3浓度增大
C. A电极的反应为:NO2-e-+H2O==NO3-+2H+ NO-3e-+2H2O===NO3-+4H+
D. 该电池工作时,每消耗11.2LO2(标准状况下),可以除去含1molNO和NO2的混合尾气
【答案】C
【解析】A、电解质溶液中是通过阴阳离子的定性移动形成电流,选项A错误;B、B电极上电极反应式为O2+4e-+4H+=2H2O,有水生成,硝酸根离子不参加反应,所以硝酸根离子的物质的量不变,但氢离子消耗减少,溶液体积增大,所以硝酸浓度减小,选项B错误;C、A电极氮的气化物失电子转化为硝酸根离子,电极反应式为:NO2-e-+H2O=NO3-+2H+、NO-3e-+2H2O=NO3-+4H+,选项C正确;D、1mol NO和NO2的混合尾气中气体含量未知,则无法确定得失电子数目,则无法知道消耗氧气的量,选项D错误。答案选C。

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
