题目内容
一定温度下,有可逆反应: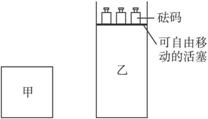
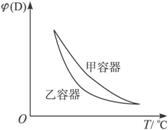
图Ⅰ 图Ⅱ
A.甲容器中的反应先达到平衡
B.两容器中的反应均达平衡时,平衡混合物中各组分的体积百分组成相同,混合气体的平均相对分子质量也相同
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2 所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍
BD
解析:本题考查平衡状态时知识综合能力。思路如下:2 mol C和6 mol D等效于4 mol A和4 mol B,本题是等体反应,不受压强影响,为等效平衡,甲、乙两容器中物质的浓度相等,所以到达平衡的时间一样,所以A错B对;两容器到达平衡的途径不一样,甲容器向正方向进行,放热,乙容器逆向进行,吸热,到达平衡后,甲容器比乙容器温度高,两容器达平衡后升高相同的温度,甲容器平衡体系应逆向移动,D的体积分数降低,乙容器中平衡体系应正向移动,D的体积分数升高;在甲容器中再充入2 mol A和2 mol B,等效于一次充入4 mol A和4 mol B,甲容器体积为V,乙容器体积为2V;所以平衡后甲中物质C的浓度是乙中物质C的浓度的2倍。

练习册系列答案
相关题目
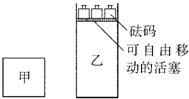 一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )
一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )| A、甲、乙两容器中的反应达到化学平衡时,两容器内压强相等 | B、甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 | C、向甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度不变 | D、向乙容器中再充入2molC和6molD,平衡后乙中物质C的浓度为原来的2倍 |



 (2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )
(2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )