��Ŀ����
����Ŀ����ԭ�ᣨC16H18O9�����нϹ㷺�Ŀ����������������������ã��������ѡ�60%�Ҵ����ݶ��ٸ�Ҷ���õ���ȡҺ����һ�������ԭ��ֲ�Ʒ��һ�ֹ���������ͼ������˵��������ǣ� ��
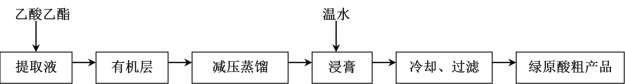
A.��ԭ������ˮ�е��ܽ��С����ˮ�е��ܽ��
B.�õ��л����ʵ�����Ϊ��ȡ��Һ
C.��ѹ�����Ŀ�ķ�ֹ�¶ȹ��ߣ���ԭ�����
D.��ԭ��ֲ�Ʒ����ͨ���ؽᾧ��һ���ᴿ
���𰸡�A
��������
��ԭ��������������������ȡҺ����������������Һ�õ��л��㣬��ѹ����õ���ԭ�ᣬ������ˮ���࣬����ȴ�����˵õ���ԭ��ֲ�Ʒ���Դ˽����⡣
A.�����м�����ˮ���࣬��ȴ�����˵õ���ԭ��ֲ�Ʒ����֪��ԭ����������ˮ��������ˮ�е��ܽ�ȴ�����ˮ�е��ܽ�ȣ���A����
B.��ԭ��Ϊ�л��ᣬ���������л��ܼ�������������������ԭ�ᱻ��ȡ���л����㣬�л�����ˮ�㻥�����ܵ�Һ��Ӧ���÷�Һ�����룬��B��ȷ��
C.��ԭ����п��������ã���ѹ����ɽ����¶ȣ������¶ȹ��ߵ�����ԭ����ʣ���C��ȷ��
D.����A�ķ�������ԭ��ֲ�Ʒ�����ؽᾧ�ķ�����һ���ᴿ����D��ȷ��
��ѡ��A��

����Ŀ��ij��ѧС��������������ƽ�������ص�ʵ�顣
����֪��Na2S2O3+H2 SO4 Na2SO4+SO2��+S��+H2O��ijͬѧ̽��Ӱ�������������ϡ���ᷴӦ���ʵ�����ʱ�����������ϵ��ʵ�飺
ʵ����� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | H2O | ||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
�� | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
�� | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
�� | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
��1����ʵ��١��ڿ�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죬���V1=V2=____��V3=___��
��2����V4=10.0��V5=6.0����ʵ��١��ۿ�̽��_____�Է�Ӧ���ʵ�Ӱ�졣
�����÷�Ӧ��I2+2Na2S2O3 Na2S4O6+2NaI�ɶ����ⶨ���������(Mr=158)�Ĵ��ȣ����ڳ�ȡwg��������ƹ�����Ʒ�����250mL����Һ��ȡ25.00mL������ƿ�У�����ָʾ������amol/L�ĵ�ˮ�ζ������ĵ�ˮb mL����
��3���ζ�ʱ������ˮע��___�����ʽ����ʽ�����ζ����У��ζ�Ӧѡ���ָʾ����____���ζ��յ������Ϊ________��
��4�����ڸõζ�ʵ����йز�������������ȷ����____��
a���ζ�ǰ��Ҫ�ö�Ӧװ�����Һ��ϴ��ƿ�͵ζ���
b���ζ������У���Һ�ε���ƿ�⣬��ʹ����õĽ��ƫ��
c���ζ���ʼʱ�ζ��ܼ��������ݣ��ζ�������������ʧ����ô��Ƚ�ƫС
d���ζ�ǰ���Ӷ������ζ�����ʱƽ�Ӷ�����������õĴ��Ƚ���ƫС
��5����Ʒ����������ƴ��ȵı���ʽΪ____��