题目内容
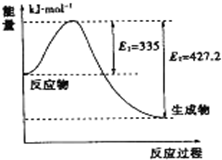
8.下列反应或过程能量变化符合图示的是( )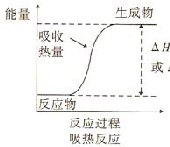
| A. | H+H→H-H | |
| B. | Mg+2HCl═MgCl2+H2↑ | |
| C. | 2Al+Fe2O3=Al2O3+2Fe | |
| D. | 2NH4Cl+Ba(OH)2•8H2O═BaCl2+2NH3↑+10H2O |
分析 生成物具有的总能量高于反应物具有的总能量,该反应为吸热反应;常见的吸热反应:C(s)+H2O(g)→CO(g)+H2O; C+CO2→CO的反应,Ba(OH)2•8H2O与NH4Cl的反应以及KClO3、KMnO4、CaCO3的分解等.
解答 解:生成物具有的总能量高于反应物具有的总能量,该反应为吸热反应.
A.新键的形成是发热过程,故A错误;
B.镁和盐酸反应是放热反应属于氧化还原反应放热,故B错误;
C.2Al+Fe2O3=Al2O3+2Fe是放热反应,故C错误;
D.Ba(OH)2•8H2O与NH4Cl的反应是吸热反应,故D正确;
故选D.
点评 本题考查化学反应的热量变化,难度不大,学生应注重归纳中学化学中常见的吸热或放热的反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.已知 HCN 的电离常数 K=6.2×10-10.用物质的量都是0.1mol 的HCN和NaCN混合后配成1L溶液,经测定溶液呈碱性.则下列关系式正确的是( )
| A. | c(CN-)>c(Na+) | B. | c(CN-)>c(HCN) | ||
| C. | c(HCN)+c(CN-)=0.2mol•L-1 | D. | c(CN-)+c(OH-)=0.1mol•L-1 |
3.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在1L 0.1mol/L的碳酸钠溶液中,氧原子总数为0.3 NA | |
| B. | 1molAl3+完全水解生成氢氧化铝胶体粒子的数目为NA | |
| C. | 常温常压下,32gO${\;}_{2}^{-}$中所含电子的数目为17NA | |
| D. | 标准状况下,11.2 L苯中含有分子的数目为0.5 NA |
13.下列说法中正确的是( )
| A. | 在25℃纯水中,c(H+)=c(OH-)=10-7 mol/L,呈中性 | |
| B. | 溶液中,若c(H+)>10-7mol/L,则c(H+)>c(OH-),呈酸性 | |
| C. | c(H+)越大,则pH 越大,溶液的碱性越强 | |
| D. | pH为0的溶液,其中只有H+而无OH- |
20.在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)═pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定能说明达到平衡状态的标志是( )
| A. | 各组分的浓度不再改变 | |
| B. | 体系的压强不再改变 | |
| C. | 反应速率υA:υB:υC:υD=m:n:p:q | |
| D. | 单位时间内m mol A断键发生反应,同时n mol B也断键发生反应 |
17.下列有关化学用语表示正确的是( )
①CSO的电子式: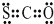
②对硝基苯酚的结构简式: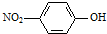
③Cl-的结构示意图: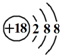
④甲烷分子的比例模型:
⑤葡萄糖的实验式:CH2O
⑥原子核内有20个中子的氯原子:${\;}_{17}^{20}$Cl
⑦HCO3-的水解方程式为:HCO3-+H2O?CO32-+H3O+.
①CSO的电子式:
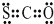
②对硝基苯酚的结构简式:
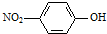
③Cl-的结构示意图:

④甲烷分子的比例模型:

⑤葡萄糖的实验式:CH2O
⑥原子核内有20个中子的氯原子:${\;}_{17}^{20}$Cl
⑦HCO3-的水解方程式为:HCO3-+H2O?CO32-+H3O+.
| A. | ③⑤⑥⑦ | B. | ②③④⑥ | C. | ①④⑤ | D. | 全部正确 |
18.下列说法正确的是( )
| A. | 在化学反应中,化学能只可以转化为热能 | |
| B. | 合成氨反应N2+3H2?2NH3,当N2、H2、NH3浓度相等时该反应达到了最大限度 | |
| C. | 合成氨反应N2+3H2?2NH3中,升高温度,该反应速率减小 | |
| D. | 化学键的断裂和形成是化学反应中能量变化的主要原因 |
 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源. 如图是中学化学中常用的玻璃仪器组成的实验装置图(根据需要可在广口瓶中加入液体或在干燥管中放入固体).
如图是中学化学中常用的玻璃仪器组成的实验装置图(根据需要可在广口瓶中加入液体或在干燥管中放入固体).