题目内容
(12分)理论上,SO2能发生类似CO2与澄清石灰水作用的反应,但在通常实验中,将SO2通入澄清石灰水却没有看到类似CO2那样先浑浊后澄清的现象。针对这一问题,研究性学习小组开展了探究性实验。

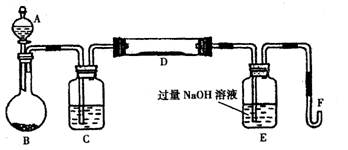
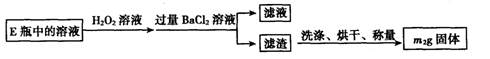
I.用图A所示的装置来分别做CO2、SO2与澄清石灰水的反应实验,结果通人CO2可看到先浑浊后澄清的现象,但通入SO2没看到浑浊现象。
Ⅱ.用图B的装置,将气体收集在注射器里,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,无论CO2还是SO2都能看到“先变浑再澄清”的现象。当以相同速率分别通人CO2或SO2,通入SO2产生现象明显比通入CO2产生现象快。
回答下列问题:
(1)通过上述I、Ⅱ实验,可以确定,将足量SO2缓慢通人澄清石灰水,依次发生的反应有:(用离子方程式表示) ; 。
(2)实验I中,通人SO2不能出现浑浊的原因可能是: 。
(3)实验Ⅱ中,同速率分别通入CO2或SO2,SO2产生现象比CO2快的相关因素有 。
①SO2在水中溶解度比CO2大。
②相同状态下,SO2的密度比CO2的密度大。
③亚硫酸酸性比碳酸强,在同温度、同体积的溶液中,l mol亚硫酸电离产生的H+离子浓度大于l mol碳酸电离产生的H+离子浓度。
④SO2有毒和刺激性气味, CO2无毒和无刺激性气味。
CO2无毒和无刺激性气味。
⑤相同条件下,1 mol SO2与足量石灰水反应生成CaSO3的速率大于1 mol CO2与足量石灰水反应生成CaCO3的速率。
⑥相同条件下,1 molCaSO3被1mol SO2(形成的H+离子)溶解形成可溶性Ca(HSO3)2
的速率大于1molCaCO3被1molCO2(形成的H+离子)溶解形成可溶性Ca(HCO3)2的速率。

I.用图A所示的装置来分别做CO2、SO2与澄清石灰水的反应实验,结果通人CO2可看到先浑浊后澄清的现象,但通入SO2没看到浑浊现象。
Ⅱ.用图B的装置,将气体收集在注射器里,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,无论CO2还是SO2都能看到“先变浑再澄清”的现象。当以相同速率分别通人CO2或SO2,通入SO2产生现象明显比通入CO2产生现象快。
回答下列问题:
(1)通过上述I、Ⅱ实验,可以确定,将足量SO2缓慢通人澄清石灰水,依次发生的反应有:(用离子方程式表示) ; 。
(2)实验I中,通人SO2不能出现浑浊的原因可能是: 。
(3)实验Ⅱ中,同速率分别通入CO2或SO2,SO2产生现象比CO2快的相关因素有 。
①SO2在水中溶解度比CO2大。
②相同状态下,SO2的密度比CO2的密度大。
③亚硫酸酸性比碳酸强,在同温度、同体积的溶液中,l mol亚硫酸电离产生的H+离子浓度大于l mol碳酸电离产生的H+离子浓度。
④SO2有毒和刺激性气味,
 CO2无毒和无刺激性气味。
CO2无毒和无刺激性气味。⑤相同条件下,1 mol SO2与足量石灰水反应生成CaSO3的速率大于1 mol CO2与足量石灰水反应生成CaCO3的速率。
⑥相同条件下,1 molCaSO3被1mol SO2(形成的H+离子)溶解形成可溶性Ca(HSO3)2
的速率大于1molCaCO3被1molCO2(形成的H+离子)溶解形成可溶性Ca(HCO3)2的速率。
(12分)


略

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目

 假设三: ;
假设三: ;
 外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2、④NaOH。
外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2、④NaOH。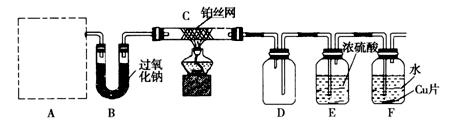
 __。
__。 ____________________________________________________________。
____________________________________________________________。
 灼热的氧
灼热的氧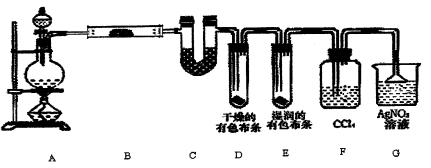
 。
。