题目内容
黄铁矿在高温时和氧气反应生成氧化铁和二氧化硫。某化学学习小组对黄铁矿石进行如下实验探究:
[实验一]:测定硫元素的含量
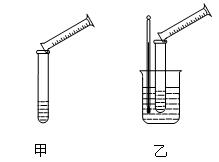
I.将m1g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的硬质玻璃管D中,A中的试剂是双氧水。从A中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管D中的黄铁矿样品至反应完全。
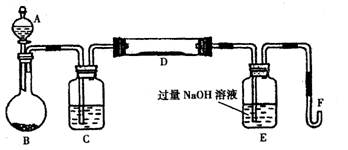
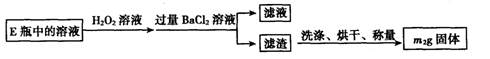
Ⅱ.反应结束后,将E瓶中的溶液进行如下处理:
[实验二]测定铁元素的含量。
Ⅲ,测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解硬质玻璃管D中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250mL;
④每次取稀释液25.00mL,用已知物质的量浓度为cmol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为VmL。
请完成下列问题:
(1)仪器B中发生反应的化学方程式是:____;仪器C中装入的试剂是____。E瓶的作用是____。
(2)Ⅱ中所加H2O2溶液需足量的理由是____;写出加入H2O2发生反应的离子方程式____。
(3)Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还有 ;④中量取稀释液25.00mL需用的仪器是__ __。
(4)该黄铁矿中硫元素的质量分数为__ __(用含m1和m2的代数式表示);该黄铁矿中铁元素的质量分数为___ _(用含m1 c、y的代数式表示)
[实验一]:测定硫元素的含量
I.将m1g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的硬质玻璃管D中,A中的试剂是双氧水。从A中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管D中的黄铁矿样品至反应完全。

Ⅱ.反应结束后,将E瓶中的溶液进行如下处理:

[实验二]测定铁元素的含量。
Ⅲ,测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解硬质玻璃管D中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250mL;
④每次取稀释液25.00mL,用已知物质的量浓度为cmol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为VmL。
请完成下列问题:
(1)仪器B中发生反应的化学方程式是:____;仪器C中装入的试剂是____。E瓶的作用是____。
(2)Ⅱ中所加H2O2溶液需足量的理由是____;写出加入H2O2发生反应的离子方程式____。
(3)Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还有 ;④中量取稀释液25.00mL需用的仪器是__ __。
(4)该黄铁矿中硫元素的质量分数为__ __(用含m1和m2的代数式表示);该黄铁矿中铁元素的质量分数为___ _(用含m1 c、y的代数式表示)

略

练习册系列答案
相关题目

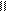 (Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。 O
(Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。 O 
 重性质。
重性质。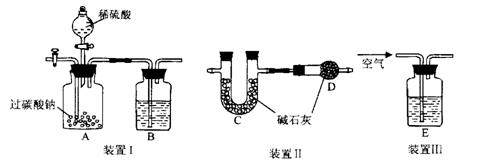
 证产生的两种气体,B中盛有足量的Ba(OH)2溶液,若观察到的现象是 ,则证明有 气体生成;简述验证另一种气体的方法 ;
证产生的两种气体,B中盛有足量的Ba(OH)2溶液,若观察到的现象是 ,则证明有 气体生成;简述验证另一种气体的方法 ; 装置III中通空气的目的是 。
装置III中通空气的目的是 。

 CO2无毒和无刺激性气味。
CO2无毒和无刺激性气味。