题目内容
【题目】我国有世界储量第一的天然石膏(主要成分CaSO4),同时也有大量磷酸工业副产品石膏,可用于硫酸及水泥的联合生产。硫酸钙在高温下被CO还原,发生的反应有:
I.CaSO4(s)+4CO(g)CaS(s)+4CO2(g) K1
II.CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g) K2
III.3CaSO4(s)+CaS(s)4CaO(s)+4SO2(g) K3
上述反应的平衡常数的对数值(lgK)与温度(T)的关系如图所示。下列说法错误的是( )
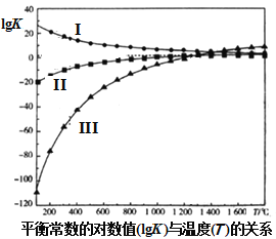
A.反应II的△H>0
B.lgK3=4lgK2lgK1
C.使用适当的催化剂能够加快反应速率,提高原料的平衡转化率
D.调控适当的温度可以抑制反应I促进反应III而得到较纯净的CaO
【答案】C
【解析】
A.lgK越大,K越大,根据图像显示,反应II升高温度lgK增大,反应II的K值增大,说明平衡正向移动,则正反应吸热反应,△H>0,故A正确;
B.利用盖斯定律,将反应Ⅱ×4反应Ⅰ得反应Ⅲ,以此可得焓变△H3=4△H2△H1,由反应转化平衡常数时,化学计量数扩大n倍,新平衡常数是原来的n次方幂,两方程式相减,新平衡常数为两者之商,两方程式相加则为两者之积,则平衡常数K3=![]() ,则lgK3= lg
,则lgK3= lg![]() =4lgK2lgK1,故B正确;
=4lgK2lgK1,故B正确;
C.使用适当的催化剂能够加快反应速率,但不影响平衡移动,则不能提高原料的平衡转化率,故C错误;
D.lgK越大,K越大,根据图像,反应I升高温度,lgK减小,说明平衡逆向移动,反应I被抑制,反应III升高温度,lgK增大,说明平衡正向移动,反应III被促进,则调控适当的温度可以抑制反应I促进反应III而得到较纯净的CaO,故D正确;
答案选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目




